Egymilliárdból is kiszúr egyetlen gyanús sejtet, kiműti a helyéről, és még az orvosokkal is cseverészik a szegedi okosmikroszkóp

„Ilyen sejtet eddig még nem láttam. És maga, professzor úr? A formája vagy a mérete alapján véli ismerősnek? Várjon, készítettem még képeket, ha esetleg nem biztos benne. Kétmillió elég lesz, vagy mutassak még?” Az MTA Szegedi Biológiai Kutatóközpontjában nem a PhD-hallgatók beszélgetnek így a kutatásvezetőikkel, hanem egy szuperokos mikroszkóp az előtte (vagy mögötte) ülő szakemberrel. Ha ebben van is némi túlzás, az legfeljebb a dramaturgiában keresendő.
Interaktív optika
Az interaktív szerkezet valójában egy rendszer, amelynek nem is egy, hanem két mikroszkóp alkotja a lelkét. A vizsgálandó szövetdarabot az első mikroszkóp nagyjából úgy pásztázza végig, mintha a világ legérzékenyebb fénymásolójába rakták volna. A mintáról több százezer, esetenként akár egymillió felvételt készít, amelyeket utóbb egy algoritmus elemez. Az önfejlesztő szoftver egyenként azonosítja a mintában az összes (akár egy-két milliárd) sejtet. Meghatározza azok alakját, méretét, sűrűségét, textúráját, majd ezek alapján mindet egyenként osztályozza, és a rá jellemző csoportba sorolja. Ha olyat talál, amelyik kilóg a sorból, megmutatja a gép előtt ülő szakembernek, és igyekszik tisztázni az általa észlelt anomáliák jelentőségét. Közben szorgosan meg is jegyzi a hús-vér kolléga szakmai véleményét, hogy legközelebb, ha nem szükséges, ne zaklassa a kérdéseivel.

A képalkotáson alapuló diagnosztikát és a mesterséges intelligenciát házasító, ekként az egész világon egyedülálló mikroszkópjuk működési elvéről a szegedi bioinformatikusok a Nature Communications című szaklapban számoltak be. Amellett, hogy az okosmikroszkóp segítségével a hazai kutatóközpontban a világ bármely pontjáról hozzáférhető sejtkönyvtárat igyekeznek létrehozni, a rendszernek jócskán akad gyakorlati haszna is – mondta a Qubitnek a szegedi kutatócsoportot vezető Horváth Péter. A szokatlannak tűnő sejteket a szoftver nemcsak kiszúrja, hanem ki is tudja vágni a mintából. A „szövetszabászatot” már egy másik – Horváth Péter szerint leginkább egy CNC-szerszámgéphez hasonlítható, ugyancsak komputerizált – mikroszkóp végzi, egy lézerkés segítségével.
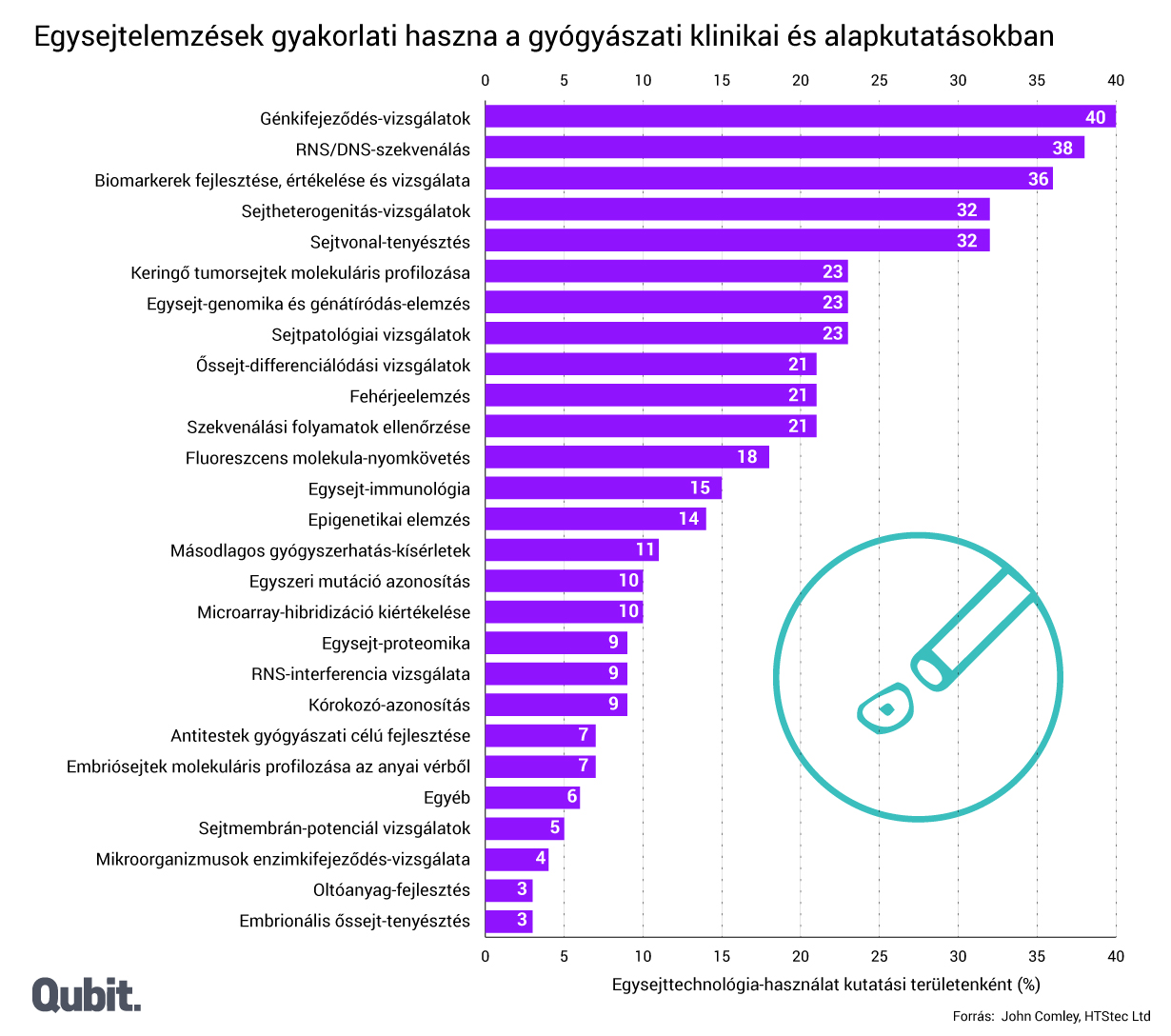
Az egysejt-elemzésnek egyelőre elsősorban az alapkutatásokban van fontos szerepe, de szép számmal akadnak, akik a gyakorlati gyógyászatban is örömmel látnának a szegediekéhez hasonló mikroszkópokat – ma még főleg diagnosztikai céllal. A lombikbébi-programok során például az osztódó embrióból ki lehetne választani egy sejtet, amelynek az örökítőanyagában már a beültetés előtt fel lehetne fedezni az esetleges genetikai hibákat. Az efféle eljárások során meglehetősen gyakori génhibák korai szűrésével például meg lehetne kímélni a pácienseket a többszöri vetéléstől.
Mit tehet a sejt?
Különben is legfőbb ideje lenne, hogy a kutatóorvosok által az ezredforduló óta gyakran emlegetett paradigmaváltás magasabb fokozatra kapcsoljon. Közel két évtizede elmélkednek arról, hogy a szervezet génállományának a teljességét sejtszinten vizsgáló genomika és ugyanezt az alaposságot a sejtek által gyártott fehérjekészlet vizsgálatára is kiterjesztő proteomika térnyerésével személyre szabottá válik majd az orvoslás. Csakhogy a gyógyítás alapkövének a szervek és a szövetek helyett a sejteket tekintő molekuláris medicina többnyire még ma is legfeljebb csak a laboratóriumokban létezik.
Az újfajta medicina rohamszerű terjedésének az egyik legnagyobb gátját mindjárt az újdonsült „páciensek”, az individuális sejtek előteremtése jelenti. Pedig a szöveteket alkotó, vagy épp az oda – például daganatsejtek formájában – hívatlanul befurakodó sejtek szétválasztására elméletben több módszer is adódna. A mintákból elvileg ki lehet válogatni egy-egy sejtet vagy sejttípust a fizikai jellemzői – a súlya, az alakja, a sűrűsége vagy épp a membránfeszültsége – alapján. Ehhez azonban a sokféle sejtet tartalmazó mintákat többnyire folyékony közegben kell előkészíteni, vagyis ki kell szakítani az eredeti környezetéből. Az efféle kísérletekből pedig rendre az derül ki, hogy a sejtek önmagukban mégsem szolgálnak elég információval. Ahhoz, hogy azokra bármilyen, pláne személyre szabott terápiát lehessen építeni, arra az információra is szükség lenne, hogy pontosan honnan kerültek elő, kik voltak a szomszédaik, azokkal milyen viszonyt ápoltak. A véráramban keringő, onnan véletlenszerűen egy kémcsőbe kerülő sejtből pedig sok minden kiderül ugyan, de az nem, hogy merre járt és mit csinált a vérvétel előtti percekben.

Kivágták magukat
Ezt a gordiuszi csomót vágta át sikeresen a szegedi mestereséges intelligencia. A tárgylemezenként akár milliónyi felvételt is elemző szoftver az eredeti környezetükben monitorozza a sejteket, majd szükség esetén a lézer is előkészítés nélkül, az eredeti mikrokörnyezetükből távolítja el a sejteket. Más kérdés, hogy a lézerkéseknek nincs túl jó hírük a sejtek molekuláris szintű vizsgálatára szakosodott kutatók körében. Túlságosan nagy ugyanis a veszélye, hogy a „vágás” nyomán megsérülnek a vizsgálandó molekulák. Az eddigi vizsgálatok alapján az okosmikroszkópba szerelt, a fény láthatóság alatti tartományában működő úgynevezett hideglézer amellett, hogy 1 mikron pontossággal vág, kíméletes a sejtalkotókhoz – mondja Horváth Péter. A kiemeléskor pedig amúgy is a sejt széléhez közel „metszenek”. És ha mindez nem lenne elég: miután a kutatócsoport legfontosabb újítása a mesterséges intelligencia bevetése volt, máris azt vizsgálják, hogyan lehetne az algoritmussal a lézer helyett kíméletesebb módszereket, például szippantást alkalmazni.