Hasznos élesztők: mérföldes lépésekkel haladunk a dizájner-probiotikumok felé


Az emberi mikrobiom az egyes testtájakat benépesítő természetes mikróbaközösségek összefoglaló neve, ezek legnagyobb része pedig a gasztrointesztinális traktusban, a bélflórában található. A mikrobiom baktériumai és egyéb mikroorganizmusai számos fiziológiás folyamatot befolyásolnak, így rendkívül nagy hatással vannak egészségünkre. A bélflórának kritikus szerepe van az immunrendszer fejlődésében, gátolja a patogén mikroorganizmusok elszaporodását, szabályozza a bél endokrin funkcióit, de még az idegrendszer jelátviteli folyamatait is, valamint részt vesz egyes vitaminok szintézisében. A baktériumokon kívül a mikrobiom tagjai között találunk úgynevezett archeonokat (amelyeket korábban helytelenül ősbaktériumként emlegetett a csekély számú magyar szakirodalmi munka), vírusokat és eukariótákat, közöttük pedig magasan a gombák különböző fajai dominálnak. A gomba-mikrobiomot szokás mikobiom néven is emlegetni.
A csecsemőkéhez képest a felnőttek mikrobiomja stabil, de bizonyos fajok és alfajok, valamint ezek arányai eltérést mutatnak személyenként, népcsoportonként, illetve tucatnyi más szempontból. Az időseknél a bélflóra fajösszetétele instabil és kevésbé sokszínű, így az idős kor elérésével az immunkompetencia csökken. Számos tanulmány vizsgálta egyes betegségek kialakulása szempontjából a mikrobiom szerepét, ezek között kiemelt szerepet foglalnak el a gyulladásos betegségek (irritábilis bél szindróma, IBS és gyulladásos bélbetegség, IBD). Az IBD két fő típusa a fekélyes vastagbélgyulladás és a Crohn-betegség. Megfigyelték, hogy egyes baktériumok és gombák kölcsönhatása hozzájárulhat az IBS kialakulásához, míg mások enyhíthetik azt. A mikrobiom módosítása többek között probiotikumok felhasználásával ezek alapján potenciális kezelési megoldás lehet a gyulladásos bélbetegségben szenvedőknek. A probiotikum készítmények hagyományosan tejsavtermelő baktériumokat tartalmaznak, amelyek megtalálhatóak a humán gasztrointesztinális traktusban. Azonban nem csak baktériumok rendelkeznek probiotikus hatásokkal, hanem a bor- ill. pékélesztő, vagyis az élesztőgomba, a Saccharomyces cerevisiae faj egyes törzsei is. Ezek közül is kiemelkedik a Saccharomyces boulardii altípus, mely a leghosszabb ideje forgalomban lévő és leginkább vizsgált probiotikus gomba.
A S. boulardii-t az akut és krónikus gasztrointesztinális betegségek esetén is hatékonyan lehet alkalmazni kiegészítő kezelésként. Jelenleg ez az egyetlen élesztő, ami probiotikumként kereskedelmi forgalomban kapható Magyarországon: a S. boulardii CNCM I-745 törzs probiotikus tulajdonságait több mint 80 randomizált klinikai vizsgálat igazolja. A S. boulardii-t Henri Boulard francia mikrobiológus fedezte fel 1920-ban Indokínában, ahol fermentálási folyamatokban felhasználható élesztőtörzsek után kutatott. Gyümölcsök héjáról izolált egy élesztőt, amiről a helyiek szokásait megfigyelve feltételezte, hogy probiotikus hatása megakadályozza a kolerafertőzést, illetve csökkenti a betegség tüneteit. Azóta is az általa izolált élesztőket használják probiotikumok gyártásához, és csak az utóbbi években kezdett bele több cég és kutatócsoport is alternatív élesztőtörzsek keresésébe és fejlesztésébe.
A fajok nevezéktanához kapcsolódó érdekesség, hogy a S. boulardii-t csak évtizedekkel felfedezése után próbálták meg leírni különálló fajként, azonban ezt nem a nómenklatúra szabályai szerint tették. Így a probiotikum élesztők latin neve invalid név, jelenleg leginkább a termék megkülönböztetését szolgálja. A faji vagy alfaji megkülönböztetés azért sem indokolt tudományos szempontból, mert a S. boulardii törzsek egytől egyig a S. cerevisiae (pék- ill. borélesztő) faj európai fejlődési ágának egyik alcsoportjába tartoznak, nem alkotnak jól elkülönülő ágat a faj törzsfáján.
A S. boulardii optimális növekedési hőmérséklete 37°C, képes túlélni a gyomorban és a bélben. A probiotikumos kezelés megszakításától számítva viszonylag gyorsan, 3-5 nap elteltével kiürül a szervezetből. Fontos azonban megjegyezni, hogy ez az élesztőfaj ritkán képes maga is fertőzést okozni, és a bélből kiszabadulva a keringési rendszerben vagy más szervekben kórokozóként szaporodni. Használata így immunszupresszált, illetve kritikusan beteg személyeknél ellenjavallt – egy belga kórház (a brüsszeli Saint-Pierre egyetemi kórház) pedig éppen a biztonságosságával kapcsolatban felmerült aggályok miatt be is szüntette forgalmazásáta a kórházi gyógyszertárban. A Debreceni Egyetemen működő kutatócsoportunk a közelmúltban publikált egy, a probiotikus élesztőkből származó fertőzések diagnosztikájára alkalmas gyors genetikai módszert, amely kimutatta, hogy a pék- ill. borélesztő mint faj által okozott (meglehetősen ritka) fertőzések jelentős részéért a probiotikum felelős.
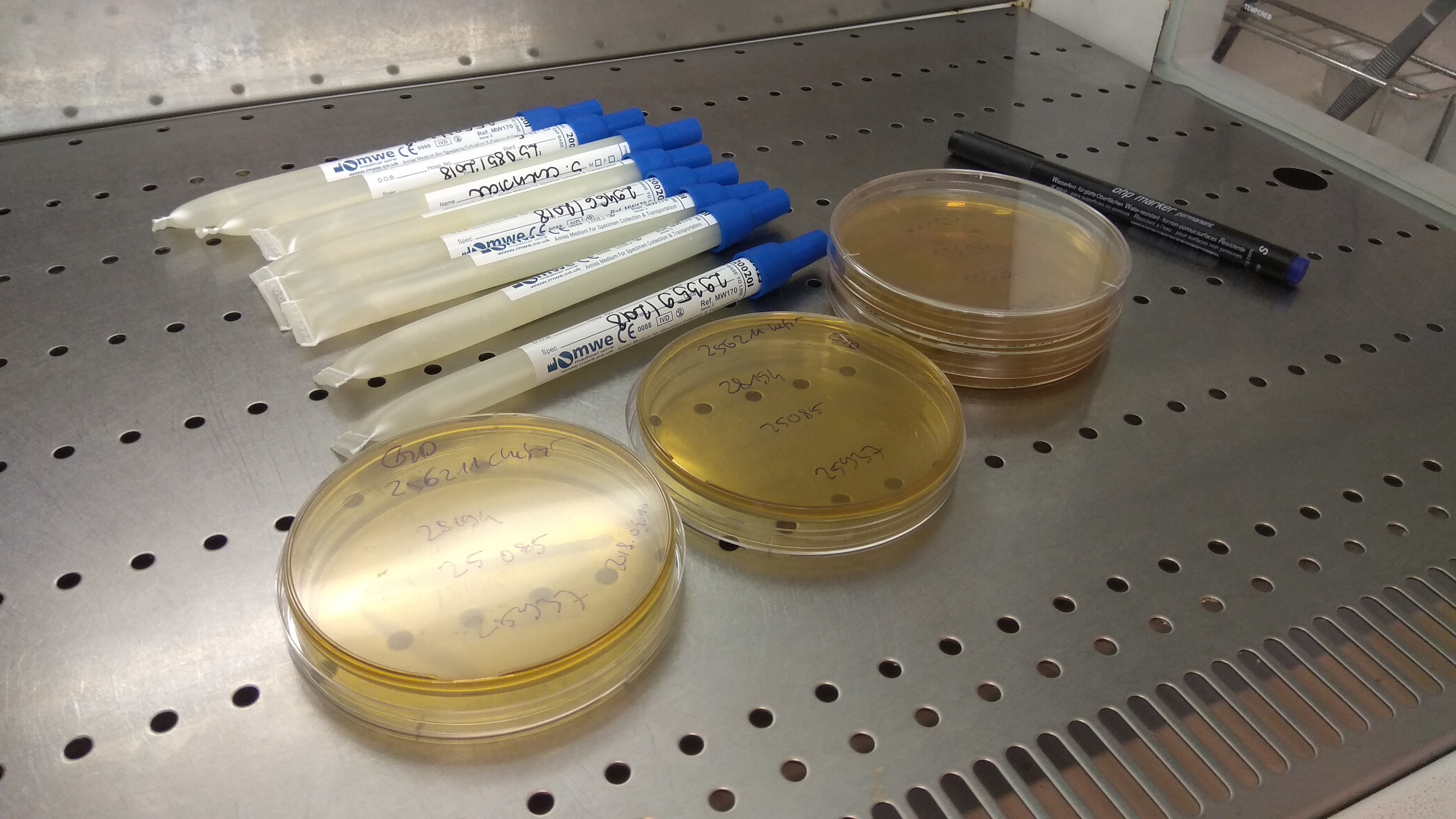
Ezeket az eredményeinket nemrég a humán és termékeredetű élesztőizolátumok teljes örökítőanyagának, azaz genomjának elemzésével is megerősítettük. Eredményeink szerint a korábban Nyugat-Európából jelentett probiotikus élesztőfertőzésekből származó izolátumok, az Európa és az USA különböző részeiből származó termékekben jelen lévő élesztőgombák és a hazai fertőzésekből szerzett minták mind rendkívül közeli rokonai egymásnak, genomjaikban nem találhatók lényeges eltérések. Más szavakkal biztos, hogy ezek a fertőzések ténylegesen a piaci forgalomban kapható termékekből indultak ki. A probiotikumok csoportja, azaz kládja közeli rokona a csak emberi mintákból ismert ún. Y’ amplifikációs kládnak (ebben a csoportban olyan élesztőgombák vannak, amelyek kromoszómái végén az élesztőkre jellemző Y’ szakaszok szokatlan többlete jellemző). Ide tartozó élesztőgombákat Magyarországról még nem jelentettek, bár Európa több országából is ismertek kórokozóként. Szintén közeli rokon csoport a borélesztők egy alcsoportja, ahivá hazai humán minták is tartoznak. Ebben a csoportban korábban csak a természetből, növényekről származó izolátumok voltak ismertek, kereskedelmi forgalomban árult borélesztőkkel ezek nem mutattak rokonságot. A hozzájuk köthető humán fertőzések kialakulásának körülményei ismeretlenek.
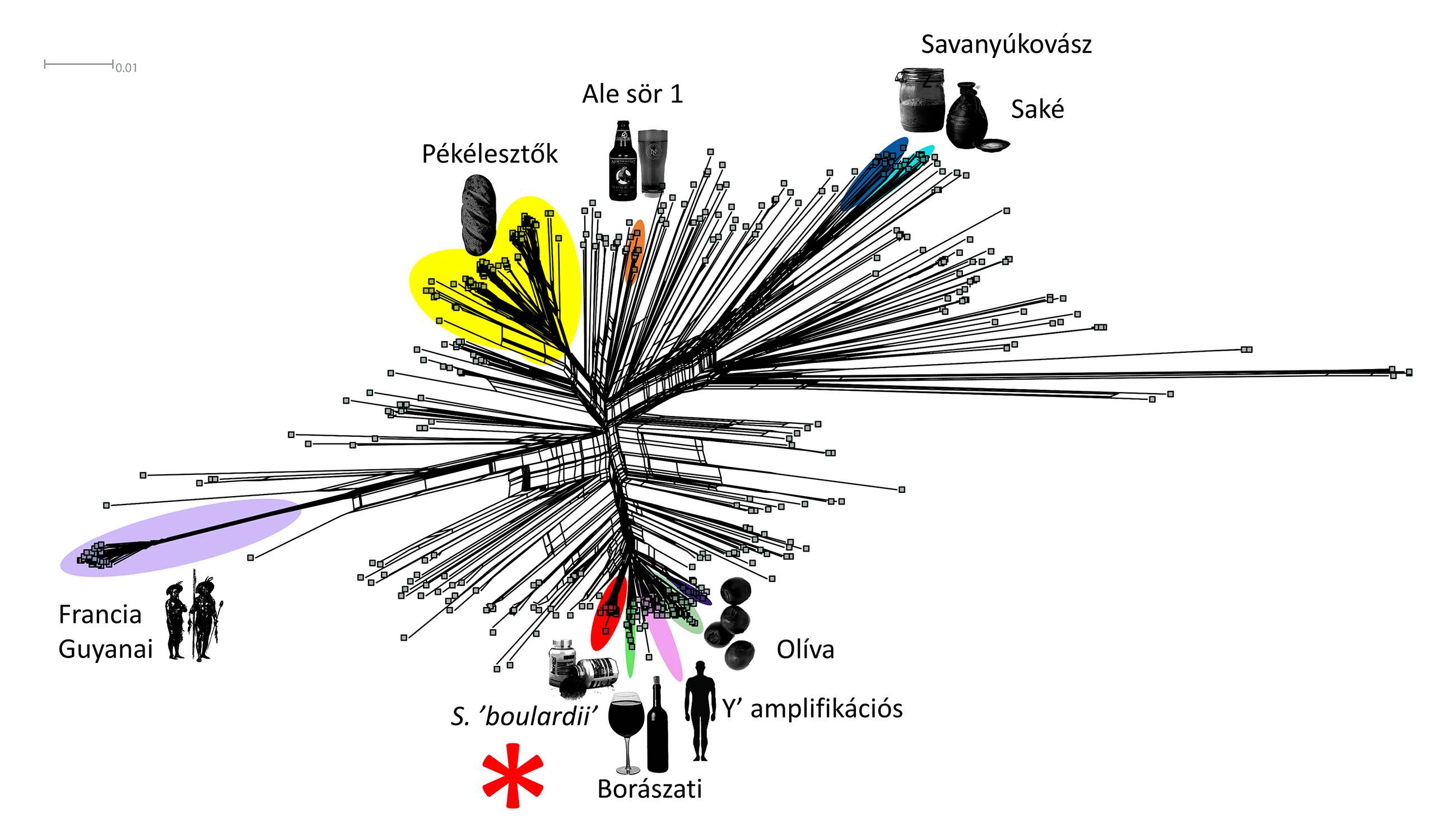
A S. boulardii-val foglakozó tanulmányok túlnyomó többsége magától értetődő módon a probiotikus élesztők előnyeire fókuszál, és nem a ritkán okozott mellékhatásokra, vagyis az élesztőfertőzésekre. Az IBS-re gyakorolt hatásukat vizsgáló tanulmányok megállapították, hogy a gomba növelni képes a bél úgynevezett barrier funkcióját, csökkenti a gyulladás mértékét, valamint a hasmenést is enyhíti. Ezen hatások pontos mechanizmusa azonban nem ismert. Nemrégiben azonban a probiotikus élesztőkkel foglalkozó kutatói közösség azonban felismerte, hogy fontos a hatásmechanizmusok beható megértése, sőt, pontos szabályozhatósága. A fókusz így a molekuláris biológia új ága, a szintetikus biológia felé fordult. A probiotikus és egyéb élesztőket ma már rutinszerűen tudják genetikai módosításokkal úgy alakítani, hogy szabályozható módon termeljenek akár más élőlényekből származó molekulákat is. Néhány héttel ezelőtt a Nature Medicine folyóiratban jelent meg amerikai és kanadai szerzők tanulmánya egy olyan kutatásról, amit a Harvard Egyetem orvosi karának Brigham and Women’s Hospital intézete irányított. Ebben önszabályozó élesztőket hoztak létre, amelyek az IBS egyik gyulladásos jelmolekuláját, a sejten kívüli adenozin-trifoszfátot (eATP) érzékelik, majd érzékelő rendszerük aktiválásakor a gyulladásos molekulát semlegesítő enzimet termelnek. Az élesztő hatásosságát egérkísérletek is igazolták. Az eATP-t a mikrobiom tagjai és az aktivált immunsejtek is termelik (bél)gyulladás esetén. Ez a molekula gyulladási citokinek termelését segíti elő, aktiválja az effektor T-sejteket, és serkenti a bél idegsejtjeinek programozott sejthalálát, vagyis hozzájárul az IBD tüneteinek kialakulásához, súlyosbodásához. A tanulmányban leírt dizájner, azaz programozható probiotikum felületére egy olyan módosított receptormolekula került, amely az emberi sejteken érzékeli az eATP-t. Ezt a receptort a kutatók ráadásul az irányított evolúció eszköztárának segítségével úgy módosították, hogy nagyon kis koncentrációban is reagáljon az eATP-re: a receptor génjébe véletlenszerű mutációkat vittek be, majd a receptorváltozatokat termelő élesztők közül kiválasztották a legérzékenyebbet. Ezt az tette lehetővé, hogy az eATP-kötés által egy szintén mesterségesen létrehozott jelátviteli út megkezdte egy vörös fluoreszcens fehérje termelését – így a legvörösebb élesztőkről tudni lehetett, hogy nagy mértékben reagálnak az eATP-re.
Végeredményben akár ezerszer érzékenyebb receptorok kifejlesztésére került sor. Ezt az érzékenyebbé tett receptort a kutatás következő szakaszában arra használták, hogy vörös fluoreszcens fehérje helyett egy terapeutikus válaszelemhez kössék az eATP érzékelését és az arra épülő szintetikus jelátviteli rendszert. Ehhez egy újabb organizmus egyik génjét használták fel: a burgonya egyik apiráz enzimjét kódoló szakaszt vittek be az élesztőbe. Az apiráz enzim az eATP-t elhasítja, a keletkező adenozin pedig egyenesen immunszupresszív hatású. A bevitt génen is alkalmaztak módosításokat, többek közt azért, hogy az élesztő ezt az enzimet majd a sejten kívülre juttassa, ahol kifejtheti hatását. Az így létrehozott élesztőtörzset bélgyulladásos egerekbe juttatták, ahol életben maradt, és reagált az eATP-re, elbontva azt. A dizájner probiotikummal való kezelés hatásossága hasonló volt a hagyományosabb, antitest alapú kezeléséhez. A probiotikus élesztők jelenléte ugyanakkor nem változtatta meg számottevően az egerek mikrobiomját sem, ami szintén pozitívum.
A jövőben várható tehát, hogy a probiotikus készítmények legalább egy része a szintetikus biológia eszköztára által rájuk ruházott tulajdonságokkal gyógyít majd minket. Emellett egyes szintetikus biológiai módszereket már most adaptálni terveznek a kórokozó baktériumok bélből való kiirtására is. Ez a módszer hatékonyabb és célzottabb kezelést ígér, mint amit az antibiotikumokkal elérhetünk. Az ilyen új, szintetikus biológiára épülő mikroorganizmusok felhasználása teljesen új távlatokat nyit, biztonságosságuk megfelelő felmérése és a jogi környezet szabályozása után (hiszen genetikailag módosított mikrobákról van szó) pedig előbb-utóbb a mindennapi gyógyításba is bekerülhetnek.
Felhasznált források
- Imre A, Rácz HV, Antunovics Z, Rádai Z, Kovács R, Lopandic K, Pócsi I, Pfliegler WP. A new, rapid multiplex PCR method identifies frequent probiotic origin among clinical Saccharomyces isolates. Microbiol Res. 2019; 227:126298. doi: 10.1016/j.micres.2019.126298.
- Pais P, Almeida V, Yılmaz M, Teixeira MC. Saccharomyces boulardii: What makes it tick as successful probiotic? J Fungi (Basel). 2020; 6(2):78. doi: 10.3390/jof6020078.
- Poncelet A, Ruelle L, Konopnicki D, Miendje Deyi VY, Dauby N. Saccharomyces cerevisiae fungemia: Risk factors, outcome and links with S. boulardii-containing probiotic administration. Infect Dis Now. 2021; 51(3):293-295. doi: 10.1016/j.idnow.2020.12.003.
- Scott BM, Gutiérrez-Vázquez C, Sanmarco LM, da Silva Pereira JA, Li Z, Plasencia A, Hewson P, Cox LM, O'Brien M, Chen SK, Moraes-Vieira PM, Chang BSW, Peisajovich SG, Quintana FJ. Self-tunable engineered yeast probiotics for the treatment of inflammatory bowel disease. Nat Med. 2021; 27(7):1212-1222. doi: 10.1038/s41591-021-01390-x.
A cikk szerzőiről
Pfliegler Valter a Debreceni Egyetem Molekuláris Biotechnológiai és Mikrobiológiai Tanszékének adjunktusa, kutatási területe a különböző gombafajok, elsősorban az élesztőgombák evolúciója, diverzitása, fertőzőképessége, a gombák szerepe a mikrobiomban. A Saccharomyces cerevisiae élesztőfaj háziasításával, genomevolúciójával és potenciális patogenitásával kapcsolatban 2021 szeptemberétől az NKFIH Fiatal Kutatói pályázatának támogatásával kutatócsoportot vezet.
Imre Alexandra a Debreceni Egyetem Laki Kálmán Doktori Iskolájának végzős doktorandusza, kutatásában az élesztőgombák, kifejezetten a probiotikus S. boulardii élesztő geno- és fenotípusos jellemzőivel, az általa okozott fertőzésekkel, és a probiotikum élesztők genetikai módosításával foglalkozik. A probiotikus élesztőkkel kapcsolatos projektjét az induló NKFIH kutatócsoportban viszi tovább.
A cikk az Innovációs és Technológiai Minisztérium ÚNKP-20-5 kódszámú Új Nemzeti KIválóság programjának a Nemzeti Kutatási, Fejlesztési és Innovációs Alapból finanszírozott szakmai támogatásával készült.
Kapcsolódó cikkek a Qubiten:
Ismerkedj meg a több milliárd jófej lakótársaddal – a csodálatos mikrobiom
A mikrobiomként emlegetett élő, egy-egy szervezetben 1 és 2,5 kiló közöttire becsült tömeget egyes kutatók már az emberi szervek közé sorolják. Mostanában kezd kiderülni, mennyire fontos szerepe van nemcsak a testi folyamatokban, de akár az idegrendszer működésében is.

A mikrobiom lehet a kulcsa annak, hogy az emberiség le tudta igázni a bolygót
A gyomorsav pH-ja, a belek hossza és mikroorganizmusainak összetétele, valamint az élelmiszerfeldolgozás egyaránt hozzájárult ahhoz, hogy az emberi faj végleg elváljon a főemlősökkel közös ősétől, és a bolygó minden szegletében megtelepedjen.
Székletátültetéssel sikerült visszafordítani az agy öregedését egy egérkísérletben
A bélbaktériumok és az agy működése közötti kapcsolat egyre nyilvánvalóbb: egy friss kísérletben fiatal egerek bélflóráját ültették át idősebb egyedekbe, amelyek azonnal kognitív javulást mutattak. A kutatók óvatosságra intenek, de a jelek szerint az emésztőrendszerben rejlik a fiatalság kulcsa.