Megvédheti a mikrobiomot egy új antibiotikum-jelölt, ami szinte csak a veszélyes baktériumokat öli meg

Új antibiotikum hatóanyagot fedeztek fel amerikai kutatók, amely képes volt egerekben a hagyományos gyógyszerekkel szemben rezisztens bakteriális tüdőgyulladás kezelésére, miközben megóvta az állatok bélmikrobiomját.
A Kristen Muñoz, az Illinois-i Egyetem (Urbana-Champaign) kémikusa és kollégái által kifejlesztett lolamicin hatóanyag specifikusan egyes patogén Gram-negatív baktériumokat céloz. Azáltal, hogy a szerdán a Nature folyóiratban ismertetett hatóanyag képes szelektálni a bélmikrobiom hasznos baktériumai és fertőzéseket okozó, káros törzsek között, az egyes antibiotikum terápiák nyomán kialakuló opportunista fertőzések ellen is védelmet nyújthat.
„Kezdik az emberek realizálni, hogy az antibiotikumoknak, amiket mindannyian szedünk – és segítenek leküzdeni fertőzéseket és néhány esetben megmentik az életünket – káros hatásai is vannak” – mondta Paul Hergenrother, az egyetem kémikus professzora, aki szerint a mai antibiotikumok az ártalmatlan baktériumokat is megölik a fertőzés kezelése közben. „El akartunk kezdeni olyan új generációs antibiotikumokon dolgozni, amelyek csak a patogén baktériumokat pusztítanák el, és nem a hasznosakat”.
A legtöbb jóváhagyott antibiotikum Gram-pozitív baktériumok ellen hatékony, vagy egyszerre támadja meg a Gram-pozitív és Gram-negatív fajokat. Kifejezetten utóbbiakat célzó gyógyszerekből eddig viszonylag kevés van, és azok is elpusztítják az ártalmatlan fajokat és törzseket. A kutatók ezért az AstraZeneca gyógyszercéggel közösen egy olyan új hatóanyagot fejlesztettek ki, amely a csak a Gram-negatív fajokra jellemző lipoprotein transzport rendszert (Lol rendszer) gátolja.
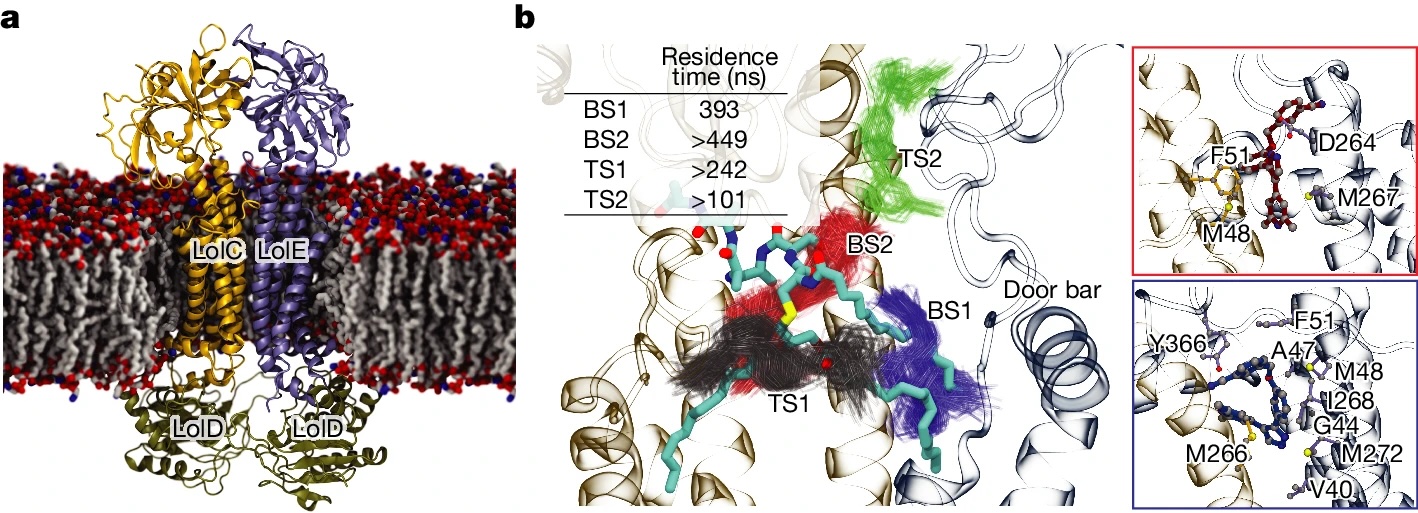
De miért csak néhány patogén baktériumot, az E. coli-t, a K. pneumoniae-t, vagy az E. cloacae-t pusztítja el az új hatóanyag? Ennek a kulcsa a kutatók szerint abban rejlik, hogy a transzport rendszerben szerepet játszó LolCDE fehérjekomplex hasonló a három faj között – miközben más Gram-negatív fajokban inkább eltér ettől. A kísérletekben a hatóanyag nagy dózisú alkalmazása a három baktériumfaj multidrog rezisztens változatainak 90 százalékát elpusztította, és a hatóanyag összességében több mint 130 multidrog rezisztens baktérium törzzsel volt képes megküzdeni.
A lolamicin azért tűnik különösen ígéretesnek, mert az egérkísérletekben a kezelés nem változtatta meg jelentősen az állatok bélmikrobiomjának összetételét, ellentétben az olyan hagyományos hatóanyagokkal, mint az amoxicillin, amelynek alkalmazása az egyetem közleménye szerint több jótékony mikroba csoport előfordulási gyakoriságát is csökkentette.
„Az egér mikrobiom jó eszköz az emberi fertőzések modellezésére, mert az emberek és az egerek mikrobiomja nagyon hasonló” – mondta Muñoz, aki szerint korábbi kutatások kimutatták, hogy a mikrobiom egyensúlyának megzavara miatt kialakuló diszbiózist okozó antibiotikumoknak hasonló hatásai vannak egerekben, mint emberekben.
Mielőtt az új antibiotikum jelölt eljuthat a klinikai alkalmazásig, még több évnyi kutatásra van szükség, köztük részletes toxikológiai vizsgálatokra. Emellett további baktérium törzsek ellen kell majd tesztelni, és azt is meg kell vizsgálni, hogy mennyi idő alatt alakul ki ellene a gyógyszerrezisztencia.
A Qubitnek május közepén Bernard L. Feringa kémiai Nobel-díjas holland kutató arról beszélt, hogy reményei szerint a következő években harcba tudunk szállni a fertőzéseket okozó, gyógyszerrezisztens baktériumok ellen okos, molekuláris gépeken alapuló antibiotikumokkal.
***
A mikrobiommal, azaz az emberi testben élő mikroorganizmusokkal és az általuk kiváltott gyulladásokkal, neurológiai betegségekkel, pszichés zavarokkal, valamint ezek kezelésével és gyógyításával foglalkozunk majd a júniusi, csak Qubit+ tagoknak meghirdetett, exkluzív tudományos estünkön, az immár nyolcadik Qubit Live-on.

Velünk lesz Schwab Richárd belgyógyász-gasztroenterológus, a Mind Klinika egyik alapítója, népszerű mikrobiom-evangelista, Oczella Péter pszichiáter, az ADHD, a skizofrénia, különböző depressziók és a demencia orvosa és Frecska Ede pszichiáter-pszichológus, az Amerikai Pszichológiai Társaság tagja, a hallucinogének és a sámáni tudatállapotok kutatója. A jegyek 24 óra alatt el is fogytak, ha a következő eseményünkről nem szeretnél lemaradni, iratkozz fel mielőbb a Qubit+-ra!
