A mikro-RNS felfedezői kapják a 2024-es orvosi Nobel-díjat

Hétfőn megkezdődött a 2024-es Nobel-hét: az orvosi (hivatalosan fiziológiai és orvostudományi) kategóriában, amelyben tavaly magyar győztest is hirdettek, az idei évben két amerikai kutató, Victor Ambros és Gary Ruvkun veheti át az elismerést, akik felfedezték a mikro-RNS-t, és annak szerepét a poszttranszkripciós génszabályozásban.
Az orvosi díjról döntő Karolinska Intézet Nobel-bizottságának indoklása szerint a két kutatónak „a C. elegans nevű apró féregben tett úttörő felfedezése a génszabályozás egy teljesen új elvét tárta fel. Kiderült, hogy ez nélkülözhetetlen a többsejtű szervezetek, így az emberek számára is. A mikro-RNS-ek alapvető fontosságúnak bizonyulnak a szervezetek fejlődése és működése szempontjából.”
Victor Ambros fejlődésbiológus kutató jelenleg a Massachusettsi Egyetem orvosi karának (UMass Chan Medical School) professzora, míg a molekuláris biológiával foglalkozó Gary Ruvkun a Harvard Egyetem orvosi karán dolgozik genetikaprofesszorként, miközben a Massachusettsi Közkórházban is kutat.
Kettejük útja akkor keresztezte egymást, amikor az 1980-as végén posztdoktori kutatásaikat végezték a Massachusettsi Műszaki Egyetemen (MIT), méghozzá a 2002-ben ugyancsak Nobel-díjjal jutalmazott Robert Horovitz kutatócsoportjában. Itt tanulmányozták a Caenorhabditis elegans nevű talajférget, amelyről kiderült, hogy alig egy milliméteres hosszúsága ellenére számos olyan speciális sejttípussal, például ideg- és izomsejtekkel rendelkezik, amelyek nagyobb, komplexebb szervezetű állatokban is megtalálhatók, így hasznos modellé vált annak vizsgálatára, hogy miként fejlődnek a szövetek többsejtű szervezetekben.
Miért fontos ez?
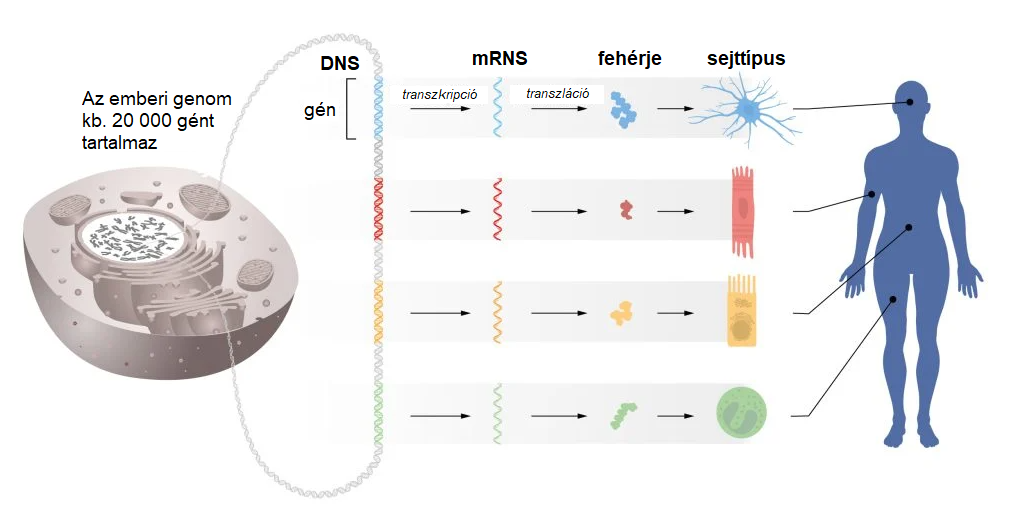
A kromoszómáinkban tárolt információ egyfajta használati utasításnak felel meg testünk összes sejtjére nézve. Mivel minden sejt ugyanazokat a kromoszómákat tartalmazza, ebből az következik, hogy minden sejt pontosan ugyanazokat a géneket és instrukciókat is hordozza magában. Ennek ellenére a különböző sejttípusok, például az izom- és idegsejtek, nagyon eltérő tulajdonságokkal rendelkeznek. Akkor mégis hogyan jönnek létre ezek a különbségek?
Erre a rejtélyre nyújt megoldást a génszabályozás, ami lehetővé teszi, hogy az egyes sejtek csak a neki szánt utasításokat hajtsa végre – azáltal, hogy biztosítja, hogy minden sejttípusban csak a megfelelő génkészlet legyen aktív.
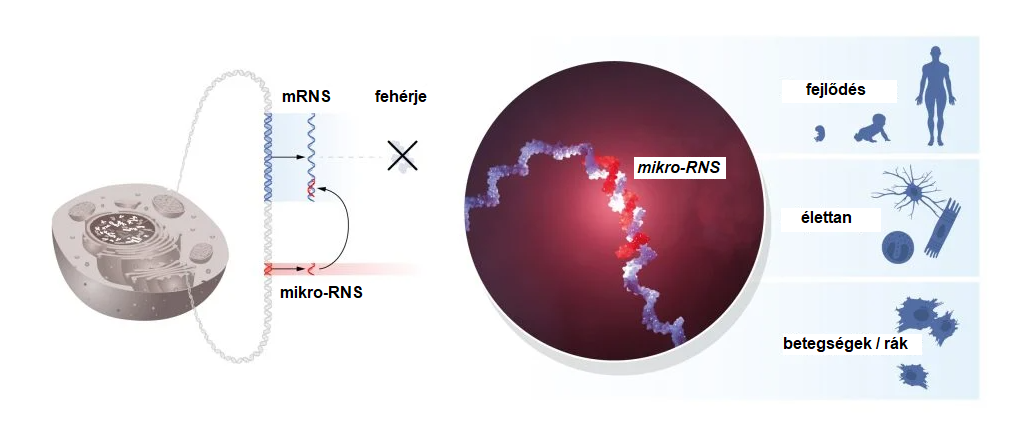
Ambros és Ruvkun a C. elegans vizsgálata során olyan géneket keresett, amelyek a különböző genetikai programok aktiválásának időzítését szabályozzák. Ehhez olyan mutáns féregtörzseket tanulmányoztak, amelyek ebben az időzítésben mutattak eltérést, majd a mutálódott gének klónozásával kimutatták, hogy azok egy szokatlanul rövid RNS-molekulát termeltek, amelyből hiányzott a fehérje előállítására szolgáló kód.
A korábban ismeretlen mikro-RNS génszabályozó mechanizmusáról szóló felfedezésüket 1993-ban publikálták a Cell folyóirat két cikkében. Eredményeik azonban nem találtak értő fülekre a tudományos közösségben, eleinte ugyanis a C. elegans sajátosságának tartották ezt a génszabályozási jelenséget, és nem gondolták, hogy más állatokra vagy akár az emberre is releváns lehet.

Egészen 2000-ig kellett arra várni, hogy ez megváltozzon: Ruvkun ekkor újabb mikro-RNS-t fedezett fel, és ezúttal egy olyan gén által kódoltat, amely az egész állatvilágban jelen van. Ennek a kutatásnak már jóval nagyobb visszhangja volt, és a következő években több száz különböző mikro-RNS-t sikerült azonosítani. Ma már azt is tudjuk, hogy az emberekben is több mint ezer gén kódol különböző mikro-RNS-eket, valamint hogy ez a fajta génszabályozás univerzális a többsejtű szervezetek között.
Ambros és Ruvkun rámutatott arra, hogy a mikro-RNS-ek általi génszabályozás már több százmillió éve része a földi életnek, és ez a mechanizmus tette lehetővé az egyre összetettebb szervezetek evolúcióját. Genetikai kutatásokból tudjuk, hogy a sejtek és a szövetek nem fejlődnek normálisan mikro-RNS-ek nélkül, és a rendellenes szabályozásuk hozzájárulhat a rák, a hallás- és látáskárosodás vagy a csontbetegségek kialakulásához is.
Mi volt eddig, és mi jön még?
Mint azt már írtuk, a fiziológiai és orvostudományi kategóriában 2023-ban magyar győzelemnek is örülhettünk: Karikó Katalint és Drew Weissmant, az mRNS-alapú oltási technológia kifejlesztői kapták a díjat. De a korábbi években elismert kutatókat és kutatásokat is részletesen bemutattuk: 2022-ben a neandervölgyi genomot megszekvenáló svéd Svante Pääbót, 2021-ben pedig a hőérzet és a tapintás receptorait felfedező David Juliust és Ardem Patapoutiant díjazta a Karolinska Intézet.
A 2024-es Nobel-díjak bejelentése kedden a fizikai, szerdán a kémiai, csütörtökön az irodalmi, majd pénteken a békedíjjal folytatódik, míg október 14-én hétfőn kihirdetik a Svéd Nemzeti Bank által 1969 óta kiosztott közgazdasági Nobel-emlékdíj győztesét vagy győzteseit is.
A Nobel-díjat Alfred Nobel svéd kémikus és feltaláló hozta létre, aki hagyatékát az emberiségnek legnagyobb hasznot hozó kutatók elismerésére ajánlotta fel – az első díjakat halála után hat évvel, 1901-ben adták át. Az elismeréseket hivatalosan idén is december 10-én, Nobel halálának napján adják majd át Stockholmban, amikor a kitüntetett kutatók a Nobel-díjhoz járó érem és diploma mellett 11 millió svéd koronát (nagyjából 390 millió forintot) is magukhoz vehetnek.


