Itt az emberi pángenom, ami soha nem látott módon képezi le fajunk genetikai sokszínűségét

Négy évnyi munka után elkészült az emberi pángenom első változata, ami minden eddiginél jobban leképezi az emberi faj genetikai sokszínűségét. A 47 egyén teljes genomjából összeállított kollekció mérföldkövet jelent a genetikai kutatásokban, és idővel hozzásegíthet betegségek jobb diagnosztikájához és kezeléséhez. A szakemberek reményei szerint a pángenom segítségével a jövőben a genomikai kutatások és a személyre szabott orvoslás vívmányai minden emberi populációnak egyaránt hasznosnak bizonyulhatnak.
Az Emberi Pángenom Referencia Konzorcium által szerdán a Nature-ben közölt eredmények a 2019-ben indult projekt első lépéseit jelentik, aminek következő célja, hogy 350 ember genomjának bevonásával kiterjesszék a fajunk genetikai diverzitását reprezentáló pángenomot. Ez, ha elkészül, a kutatók szerint lefedi majd az emberi populációkban található leggyakoribb genetikai variációkat. Továbbá a most kidolgozott módszerek más fajok genetikai diverzitásának feltérképezésében is segíthetnek.
A Qubitnek az eredményt Michael White amerikai genetikus, a St. Louis-i Washington Egyetem Genetikai Tanszékének egyetemi docense kommentálta, aki szerint a pángenom-szekvencia jelentősége óriási, de már „régóta ismert volt, hogy tovább kell lépni az eredeti emberi referenciagenomtól, amit 20 éve publikáltak”. Az új pángenom 119 millió bázispárt és 1115 génduplikációt ad a jelenleg használt, GRCh38 kódjelű, 3,1 milliárd bázispárból (bp) álló referenciagenomhoz. White szerint sokkal többet lehet majd ebből az új referenciagenomból kihozni, de időbe telhet, amíg a kutatók a pángenomot beillesztik ezt az adatfeldolgozó munkafolyamataikba (pipelines).
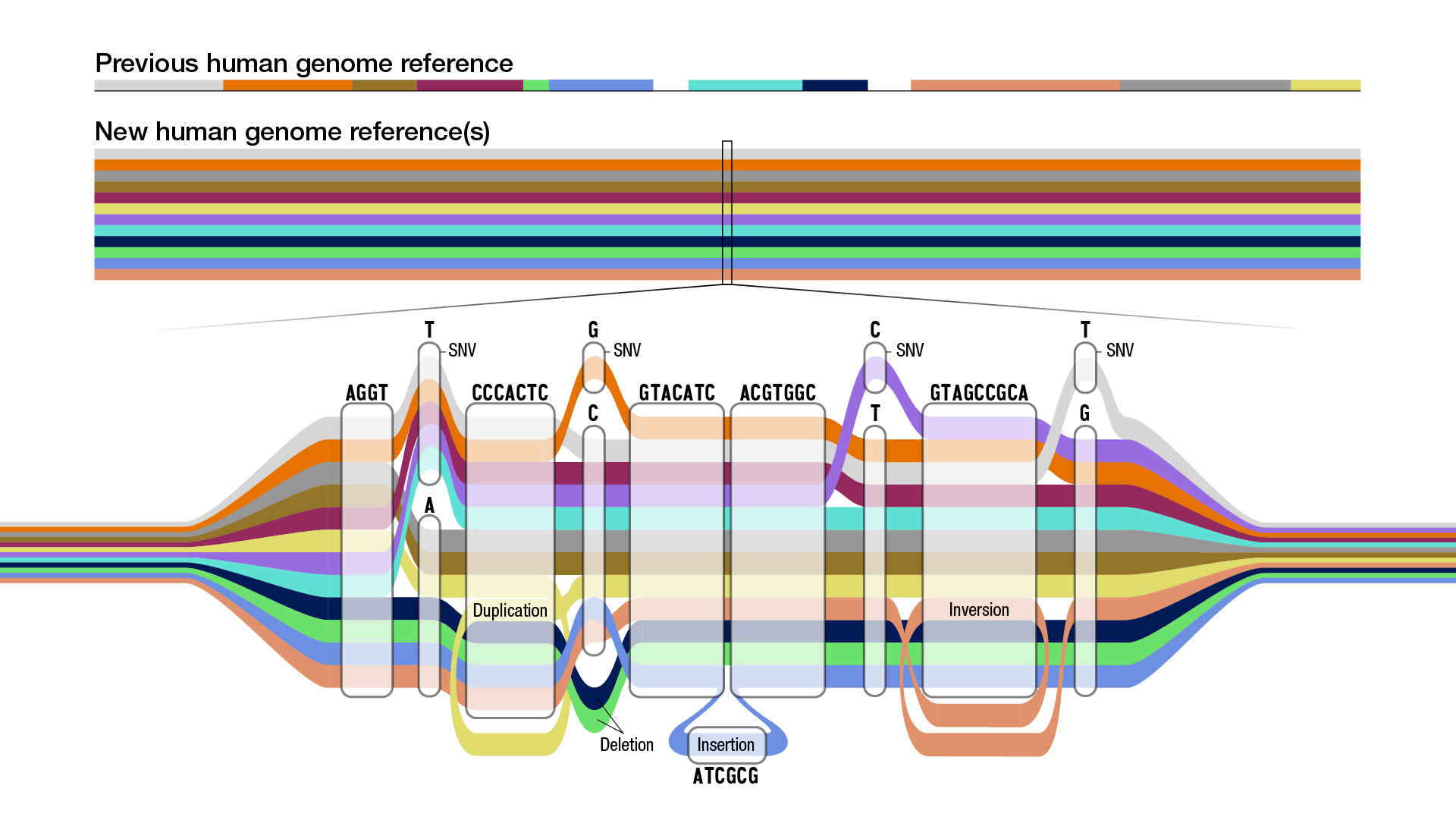
A genetikus az előrelépést a referenciagenomok szempontjából ahhoz hasonlította, mint amikor egy összecsukható flip mobilról okostelefonra váltottunk, és úgy látja, a szerzők által a legmodernebb technológiák bevetésével összeállított, nagy felbontású pángenom sokkal gazdagabban reprezentálja az emberi genetikai sokféleséget az eredeti referenciagenomhoz képest. White szerint a referencia-pángenom önmagában nem jelenít meg hatalmas változatosságot, hiszen csak 47 egyén genomját tartalmazza, főleg ha olyan projektekhez hasonlítjuk, amelyekben több százezer emberi genomot határoznak meg. Ilyen skálákon azonban szerinte ezeket a túlságosan erőforrás-igényes technológiákat nem lehet bevetni.
A pángenom értéke White szerint ezért nem abban rejlik, hogy mennyi ember genomját szekvenálták meg hozzá, hanem hogy egy jó minőségű, a korábbinál reprezentatívabb referenciaként szolgáljon. „Az új referencia-pángenom feltárja majd azt a genetikai változatosságot, ami eddig nem volt tetten érhető a nagyobb kutatásokban” az eddigi referenciagenom korlátaiból adódóan. A genetikus magyarázata szerint az, hogy meg tudjuk találni ezt a genetikai változatosságot, nagyban attól függ, hogy milyen minőségű referenciához hasonlítunk. „A 47 genommal a jelenlegi »draft« pángenom már hasznos, de a projekt terve, miszerint további több száz, mélyen karakterizált genomot adnak majd hozzá, azt jelenti, hogy a referencia-pángenom fontos eszköz lesz az emberi genetikai sokféleség megértésében az elkövetkezendő évtizedekben is” – írta White.
A legutóbbi humán genomikai áttörés a Telomere-to-Telomere (T2T) konzorciumhoz fűződik, amely tavaly közölte a Science-ben az első teljes haploid (egy kromoszómakészletet tartalmazó) emberi genomot. Ezt a pángenomot elkészítő kutatók jelentős eredménynek tartják, de hozzáteszik, hogy egyetlen genom sosem lesz képes fajunk genetikai sokféleségének leképezésére. Arya Massarat és Melissa Gymrek amerikai bioinformatikusok a Nature-nek kommentárjukban úgy fogalmaznak, hogy fajunk genetikai diverzitását ehelyett egy gráfalapú rendszerrel lehet pontosabban leírni, elágazó és összeolvadó útvonalakkal.
Az egyetlen emberi örökítőanyag alapján készült referenciagenom használata torzításokat hozhat be más emberi genomokból származó szekvenciák értelmezésébe. Ennek az az oka, hogy más emberi genomok szekvenciáit a referenciához illesztik (read mapping), és a különbségekből állapítják meg a genetikai variációkat (variant calling). Massarat és Gymrek szerint mindkét folyamat különböző eredményeket adhat, ha más személy genomján alapul a referencia, különösen a genom egyes, strukturálisan összetett régióiban. Ráadásul a referenciagenomból összességében több száz millió bázispárnyi DNS hiányozhat, amelyek nincsenek minden emberben jelen. Ezeket a kihívásokat segíthet áthidalni a sok, különböző felmenőkkel rendelkező ember genomjából készült pángenom.
A nehezen vizsgálható genetikai variációk szerepét segíthet megérteni
Két további, szintén szerdán megjelent Nature-tanulmány már az új pángenomra épít. Mitchell Vollger és kollégái úgynevezett szegmentális duplikációkban (a genom több pontján előforduló, egymáshoz hasonló szekvenciák) térképeztek fel egypontos nukleotidvariánsokat (single-nucleotide variants, SNVs), amivel több millió új variánst fedeztek fel. Emellett azonosították is azt a genetikai rekombináció (genetikai szakaszok kicserélődése) során lejátszódó, génkonverziónak nevezett molekuláris folyamatot, amely miatt a tipikushoz képest ezek a szegmentális duplikációk több guanin és citozin (GC) DNS-bázist tartalmaznak.
Andrea Guarracino, a milánói Genomikai Kutatóközpont genetikusa és munkatársai pedig rekombinációs mintázatokat figyeltek meg úgynevezett akrocentrikus kromoszómák rövid karjai között, amelyek nagy régiói átfedést mutatnak egymással. Az érintett (13-as, 14-es, 15-ös, 21-es és 22-es) emberi kromoszómáknál a struktúra közepe, a centromer nem teljesen félúton helyezkedik el, így a kromoszómák rövid és hosszú karokra oszthatók. A kutatásnak most sikerült igazolnia egy 50 éves hipotézist a hasonló régiók eredetére, ami a rekombinációjukra vezethető vissza.
Az új pángenom az eddigi GRCh38 referenciagenomnál 104 százalékkal több strukturális variánst tartalmaz. Kérdésünkre, hogy miként segítheti ezek, valamint az egypontos nukleotidvariánsok könnyebb észlelése az egyes betegségek megértését vagy kezelését, White úgy reagált, hogy a „kópiaszám-variációk [copy number variants, CNVs] fontos szerepet játszanak az emberi egészségben, ehhez képest, mivel nehéz őket észlelni, elhanyagoltuk őket”. A genetikus szerint az ilyen strukturális változatok jelentős szerepet játszanak olyan neuropszichiátriai betegségekben, mint az autizmus, és az egyének között meglévő genetikai különbségek számottevő hányadáért felelnek.
Mivel ezeket a kópiaszám-variációkat eddig nem láttuk, White szerint értelemszerűen nehéz volt megérteni egyes betegségek genetikai alapjait. A kutató úgy véli, azért nem igazán értjük, hogy milyen különböző szerepeket visznek ezek a variációk az emberi megbetegedésekben, mert nem ismerjük a teljes változatosságukat az emberi populációban.
Kapcsolódó cikkek a Qubiten:

Egy genetikai folyamat módosításával sikerült lelassítani az állatok öregedését, és már az emberi alkalmazást vizsgálják
Egy új kutatás szerint minél idősebbek vagyunk, annál gyorsabban íródik át a DNS-ünk RNS-molekulákká. A Qubitnek Charles Brenner amerikai biokémikus elmondta, hogy a folyamat lelassításával állatoknál sikerült hosszabb élettartamot és egészségesebb időskort elérni, de az még odébb van, hogy gyógyszerrel lehessen lassítani az emberek öregedését.

Százezer újszülött genomját szekvenálják meg Angliában, hogy azonnal feltárják az örökletes betegségeket
A ritka genetikai betegségek diagnosztizálása ma átlagosan öt évet vesz igénybe, ami a gyerekek fejlődése mellett a családokra és az egészségügyi rendszerre is feleslegesen nagy terhet ró.
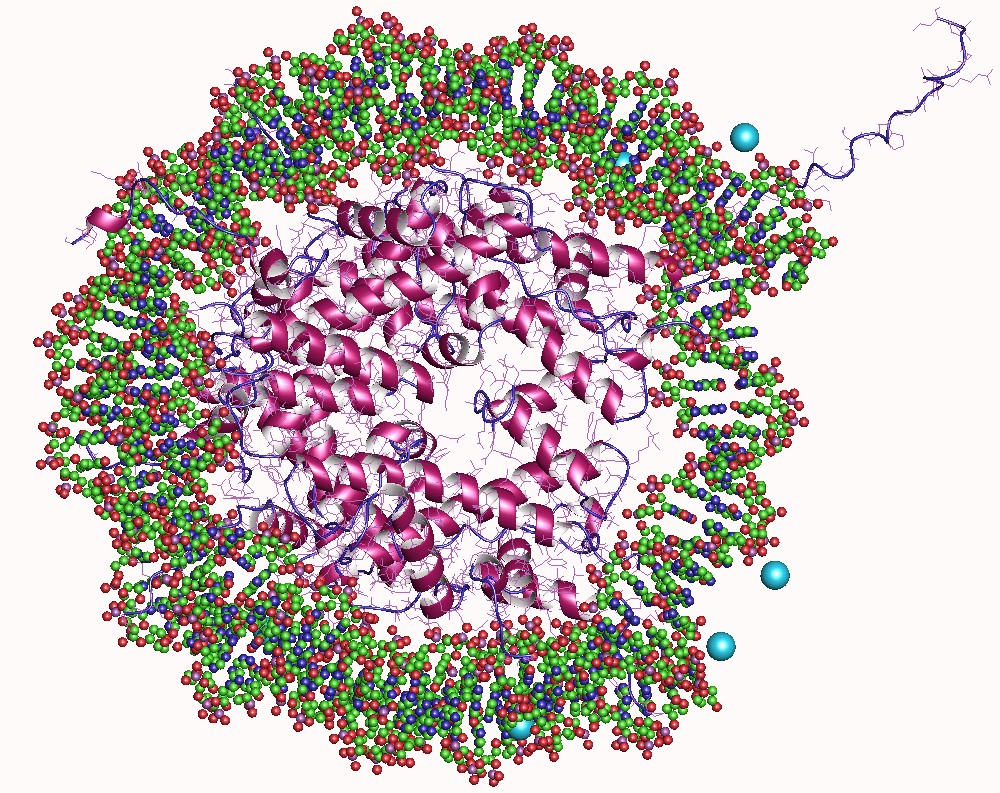
Három dimenzióban kell gondolkodnunk, ha meg akarjuk érteni a DNS működését
A genomot sejtmagba csomagoló térbeli szerkezetet és annak működését csak mostanában kezdjük igazán megérteni, de az már látszik, hogy ennek feltárása segíthet megérteni a vírusos fertőzések lefolyását és egyes betegségek okait.
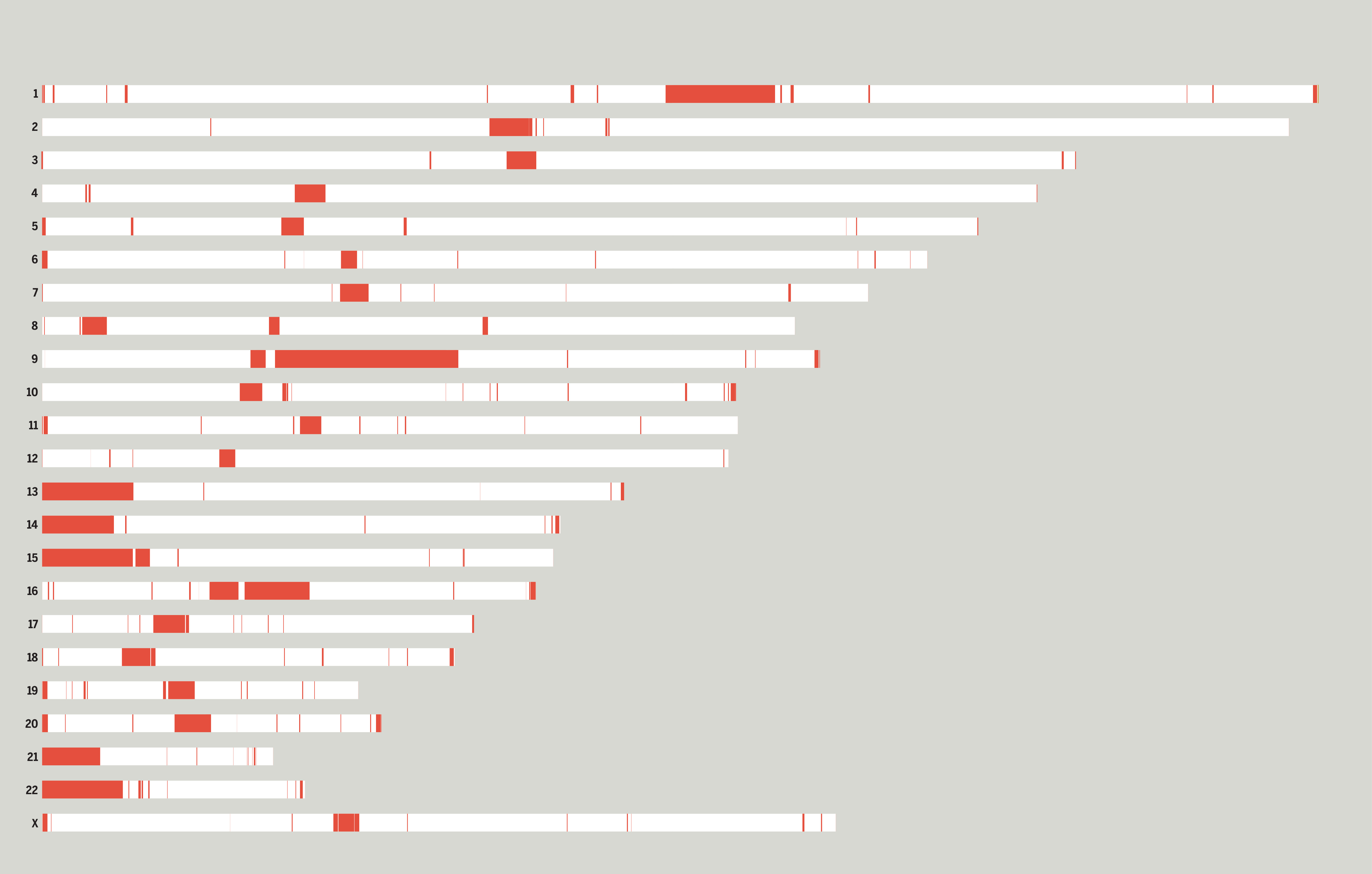
Húsz éve várt áttörés a genetikában: először sikerült hiánytalanul szekvenálni a teljes emberi genomot
A Humán Genom Projektnek 2003-ban az emberi genom 92 százalékát sikerült azonosítania, a tudósok azóta próbálták a hátramaradó 8 százalékot felderíteni. A génszekvenálási technológia fejlődésének és közel száz tudósnak hála ez mára sikerült.