Áttörést ért el a vakság gyógyításában a Roska Botond vezette kutatócsoport

„Mint aki már elgyászolta a látását, azt tudom mondani, hogy ez a kezelés tele van reménnyel” – idézte a hétfői New York Times azt az 58 éves vak embert, aki a legújabb optogenetikai eljárásnak köszönhetően újra lát.
Az eljárást kidolgozó nemzetközi kutatócsoportot Roska Botond, a bázeli Molekuláris és Klinikai Szemészeti Intézet (IOB) alapító professzora és José-Alain Sahel, a párizsi Institut de la Vision, valamint a Pittsburghi Egyetem professzora vezette. Az általuk fejlesztett optogenetikai terápiával egy retinitis pigmentosában szenvedő beteg látásfunkcióit sikerült részben visszaállítani. Klinikai vizsgálatuk eredményeit hétfőn publikálták a Nature Medicine folyóiratban.
„Ez az ember most sem tud újságot olvasni, és nem ismeri fel mások arcát sem. Ám korábban csak azt tudta megmondani, hogy jobbról vagy balról jön a fény, de azt nem, hogy milyen objektumok vannak körülötte, most viszont már objektumokat detektál. Ez az első lépés, és reméljük, hogy felgyorsulnak az események” – fogalmazott Roska professzor a kedd délelőtt rendezett online háttérbeszélgetésen.
Retina-hamburger és látás algákkal
Húsz év munkája és 13 év együttműködése érett be azzal, hogy egy 58 éves férfi, aki korábban csak úgy tudta érzékelni a fényt, mint egy amőba, most már képes a körülötte lévő tárgyak detektálásra és azonosítására – mondta a Zoom-konferencia első perceiben a budapesti születésű molekuláris és sejtbiológus, aki szerint az eredmény a vizuális rehabilitáció mérföldkövét jelenti az örökletes fotoreceptor-betegségek mutációtól független terápiáinak kifejlesztésében.
Hogy miért, annak megértéséhez először is nem árt tudni, hogy a retina olyan, mint egy biológiai számítógép, amelynek reprezentációja alapján jön létre az agy látókérgében a látás. Roska hétköznapi analógiával élve hamburgerhez hasonlította a retina funkcionális felépítését. A retina-hamburger zsömléjének teteje a fényérzékeny réteg, a saláta, a paradicsom, a sajt és a húspogácsa a számítási rétegeket jelentik, az alsó zsemlefélnek pedig a ganglionsejtek felelnek meg, ez az aggyal kommunikáló összetevő.

„Abban a legalább 250-féle betegséget jelentő tünetegyüttesben, amelyet retinitis pigmentosának hívunk, a fényérzékeny réteg megszűnik fényérzékenynek lenni, elveszíti a funkcióját. A hamburgerhasonlatnál maradva ez azt jelenti, hogy levesszük a hamburger tetejét, de ott marad a számítási és a ganglion-réteg, amely képes kommunikálni az aggyal” – magyarázta Roska.
Az 52 éves kutatónak két évtizeddel ezelőtt támadt az az ötlete, hogy nagyon egyszerű organizmusokból, például baktériumokból vagy algákból ültessenek át a fényérzékenység kifejeződésében kulcsszerepet játszó géneket az emberi retinába. Mint elmondta, azért algákból vagy mikrobákból, mert az emlősökben vagy egerekben legalább 20 gén kell ahhoz, hogy jó fényérzékenységet lehessen kialakítani. „Az ötlet megvalósításához azonban az összes technológát ki kellett fejlesztenünk, mert semmink sem volt meg hozzá”, ezért telt el olyan hosszú idő a koncepció megszületése és megvalósítása között.
Mozi a fényérzékennyé tett sejteknek
A José-Alain Sahel és Roska Botond csapatainak együttműködésében kifejlesztett optogenetikai eljárás során a ganglionsejteket genetikailag úgy módosítják, hogy azok fényérzékeny fehérjéket, úgynevezett csatorna-rodopszinokat (channelrhodopsin) termeljenek. A jelenlegi vizsgálat során a kutatók a ChrimsonR nevű csatorna-rodopszin kódoló génjét juttatták be, amelyet egy fényt érzékelni képes egysejtű algából vontak ki. Ez a különleges fehérje borostyánszínű fényt érzékel, amely biztonságosabb a retinasejtek számára, mint a más típusú optogenetikai kutatásokban használt kék fény. A kutatócsoport speciális bionikus szemüveget is kifejlesztett, amely a borostyánszínű fény hullámhosszán vizuális képeket rögzít és vetít a retinára.
„A kék fény toxikus, a borostyán már nem, de minél jobban megyünk az infravörös felé, annál jobb az eredmény, ha pedig kilépnénk a látható tartományból, akkor akár azoknál is bevethető lenne a mostanihoz hasonló módszer, akiknél nem teljes a vakság, mert abból van a legtöbb. De itt még nem tartunk” – mondta Roska. Hozzátette: „az infravörös sokkal jobb lenne, de azt a technológiát csak tavaly publikálták. Arra kell gondolni, hogy a mostani eredményhez vezető módszert 2005-ben közöltük folyóiratcikként, el kellett tehát telnie 15 évnek a megvalósításig”.
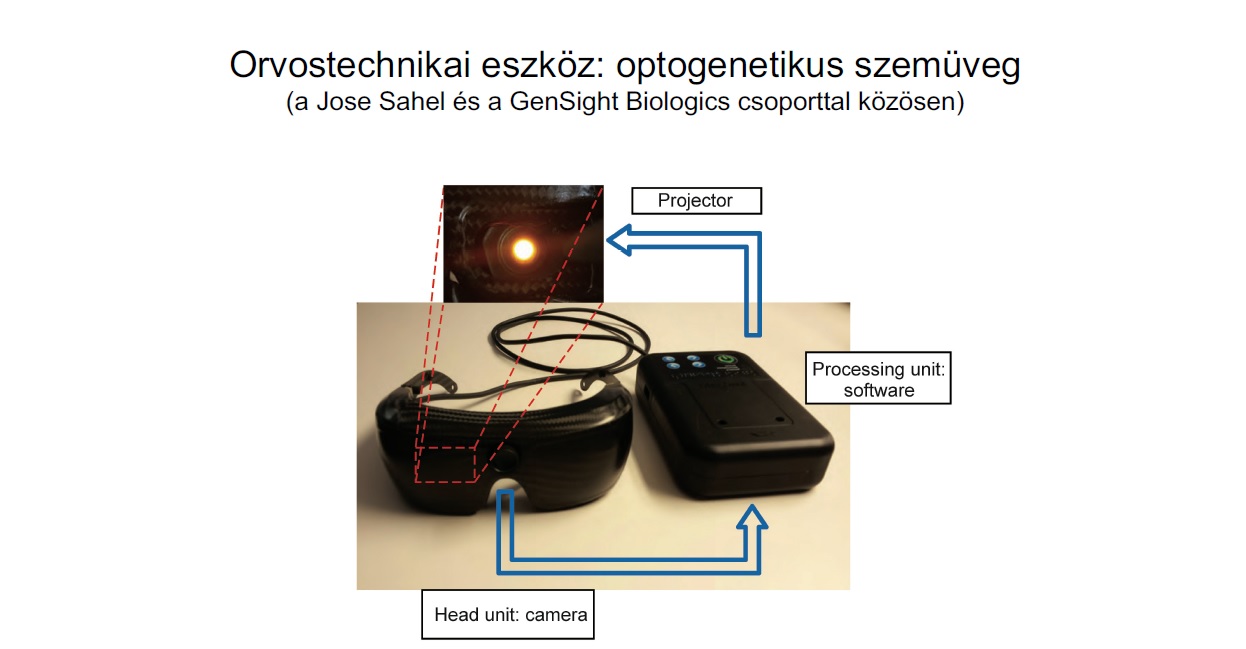
„A szemüveg egy adaptív videokamerából és egy projektorból áll, amely a szembe vetíti a fényimpulzusokat, amelyeket egy apró számítógép alakít át a videokamera felvételeiből. Fontos, hogy nem azt vetítjük rá a retinára, amit a kamera látványként felvesz, hanem azt, amiről mi azt gondoljuk, hogy a fényérzékennyé tett ganglionsejteknek szükségük van” – magyarázta Roska.
A zebra csíkjai
Az önmagában reprodukcióra képtelen asszociált adenovírusba csomagolt gén – biztonsági okokból csak az egyik szembe történt – beinjáktálása után a kutatók négy és fél hónapot vártak, így a ChrimsonR expressziójának volt ideje stabilizálódni a ganglionsejtekben.
„Ezután kezdtük trenírozni a pácienst, de két és fél hónapig nem történt semmi, amikor aztán hirtelen arról számolt be, hogy látja az utcán a gyalogátkelő csíkjait” – mondta a magyar professzor. A molekuláris biológus szerint úgy tűnik, hogy az agynak elég sok időre volt szüksége ahhoz, hogy felismerje, milyen jelzés is érkezik a szemből a látókéregbe.
A teszteredmények azt mutatták, hogy a páciens képes volt megtalálni, megérinteni és megszámolni a tárgyakat az eléje helyezett fehér asztalon, de csak a szemüveg segítségével. A szemüveg nélkül képtelen volt ezeket a gyakorlatokat elvégezni. Az egyik teszt során egy nagy füzetet vagy egy kisebb kapcsos dobozt kellett érzékelni, megtalálni, majd megérinteni. A páciens 39 különálló értékelésből 36 alkalommal (vagyis az esetek 92 százalékában) megérintette a füzetet, de a kisebb kapcsos dobozt csak az esetek 36 százalékában tudta kiválasztani. Egy második kísérletben az alany az asztalra helyezett üvegpoharakat az esetek 63 százalékában helyesen számolta meg. Egy harmadik teszt során az alany koponyasapkát viselt, amelyre elektródákat erősítettek, ezek pedig elektroenkefalográfiás (EEG) méréseket végeztek az agyi aktivitásáról.
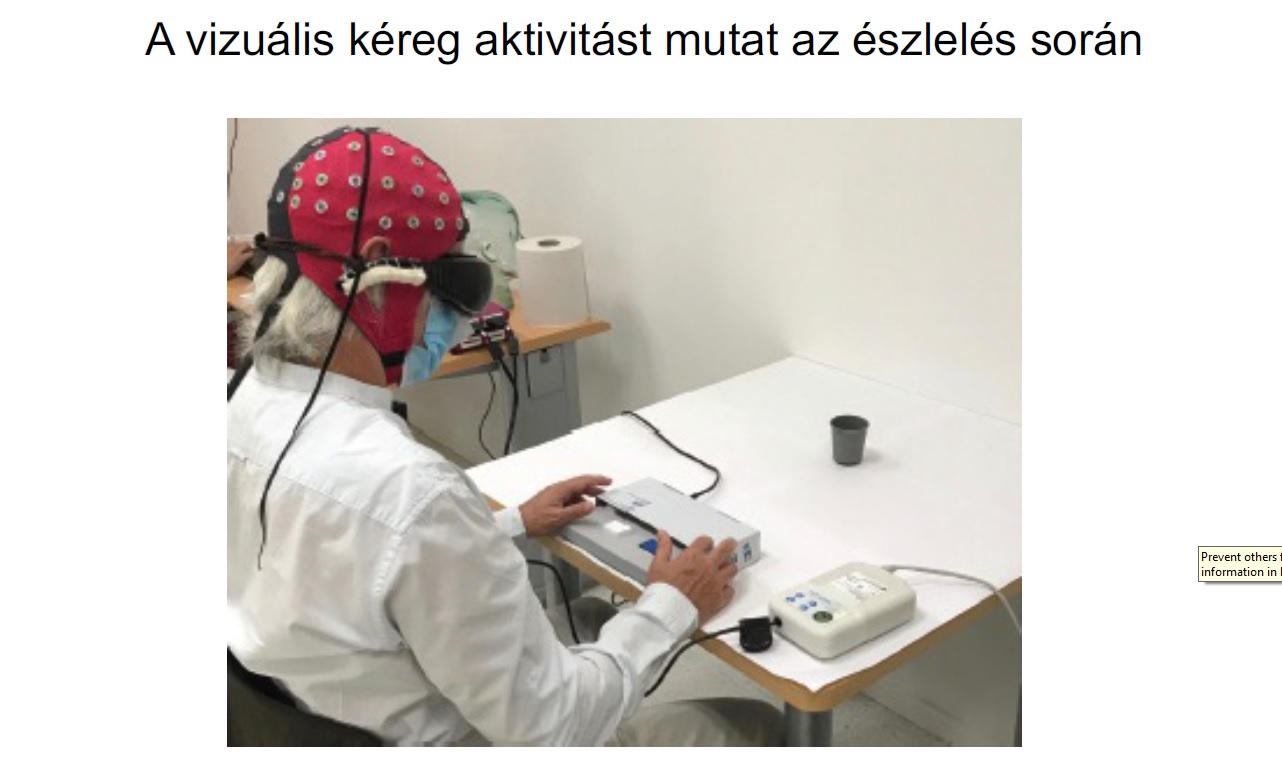
A teszt során egy poharat felváltva vettek fel vagy le az asztalról, és az alanynak egy gombot kellett megnyomnia, amely jelezte, hogy jelen van-e, vagy nincs. Fontos, hogy az EEG-mérések azt mutatták, hogy tesztelés közben az aktivitás korrelált változásai a látókéregben koncentrálódtak.
A csapat egy szoftveres dekódert is betanított az EEG-olvasások kiértékelésére. A dekóder egyszerűen a neuronális aktivitás mérésével 78 százalékos pontossággal meg tudta állapítani, hogy a pohár jelen volt-e vagy sem. Ez utóbbi kiértékelés Roska szerint segített megerősíteni, hogy az agyi aktivitás valóban egy vizuális tárgyhoz kapcsolódik, és „ezért a retina már nem vak”.
„Ez az ember már sok éve volt vak, de mivel valamikor látott, a memóriája valahogy összekapcsolódott a friss jelekkel, és elkezdett megtanulni egy új nyelvet
– hiszen a mostani aktivitási mintázatok nem egyeznek meg egy látó ember aktivitási mintázataival – magyarázta Roska. – Nekünk is meg kell tanulnunk, hogy mi is történik valójában, és azt is, hogy a bionikus szemüveg számítógépének miként kell modifikálnia a vizuális információkat ahhoz, hogy a legjobb eredményt kapjuk. Ez a következő évek kutatása lesz.”
Roska elmondása szerint a jelenlegi technológiával csak a retina közepét tudják elérni, így a mostani 58 éves páciensnek csőlátása van, tehát a fejét forgatva képes pásztázni a környezetét. „A génterápiát egyelőre csak a retina kevesebb mint 1 százalékára tudjuk kiterjeszteni, ez azt jelenti, hogy alig 10 fokot lát az illető. Két oka is van, hogy csak ekkora területet érünk el. Az egyik, hogy a retina alsó részét egy természetes membrán védi, a másik pedig, hogy az esetleges immunválaszok miatt a biztonsági előírások nem is engedélyezik nagyobb terület optogenetikai terápiáját” – részletezte a még megoldásra váró problémákat a professzor.

Fókuszban a látásromlás
Az elmúlt három évben számos fontos nemzetközi díjat elnyerő Roska 2019-ben interjút adott a Qubitnek. Ebben egyebek mellett azt mondta, „a látás azért válik egyre fontosabbá, mert nem elég, hogy az emberi agy 20 százaléka a vizuális információ feldolgozásával foglalatoskodik, a képi információ ráadásul minden eddiginél fontosabbá is vált, és ez a trend a jövőben is folytatódni fog. Mindeközben a vakok aránya a következő évtizedekben várhatóan nő majd.”
Miközben nyugaton is egyre több a rövidlátó, egyes ázsiai országokban, például Dél-Koreában mára a gyerekek 95 százaléka szorul látáskorrekcióra. A rövidlátás hosszú távon hajlamosít a retinaleválásra, valamint a makuladegenerációra, ami vakságot okoz. A vakság a szóban forgó országok lakosságának akár a harmadát is érintheti néhány évtizeden belül. „Az Egyesült Államokban nemrégiben felmérést végeztek arról, hogy az emberek milyen időskori betegségtől félnek a leginkább. A vakság megelőzte a rákot és az Alzheimer-kórt is. Ez ma a világ legrettegettebb problémája” – tette hozzá.
A professzor az interjúban az optogenetikai terápiáról is beszélt. Akkor úgy fogalmazott,
„elméletileg bármilyen szembetegségben használható a génterápia, igaz, az egyes betegségeknél másféle módon kell alkalmazni. A legegyszerűbb az úgynevezett monogenetikus betegségek terápiája, amikor a tüneteket egyetlen gén hibája okozza.”
Mint mondta, a szembetegségeknek – eltérően a többi szerv betegségeitől – elég nagy hányada ilyen. Ilyenkor az általuk fejlesztett vektorvírussal csak vissza kell juttatni a megfelelő gént a megfelelő sejtekbe, sőt van olyan öröklött monogenetikus szembetegség is, amelyre már tíz éve létezik génterápia. „Más kérdés, hogy ilyenkor problémát okozhat, hogy a hiányzó vagy hibás gének miatt a gazdasejt is elhal, így nincs hova visszajuttatni a hiányzó gént.”
Korábbi kapcsolódó cikkeink:
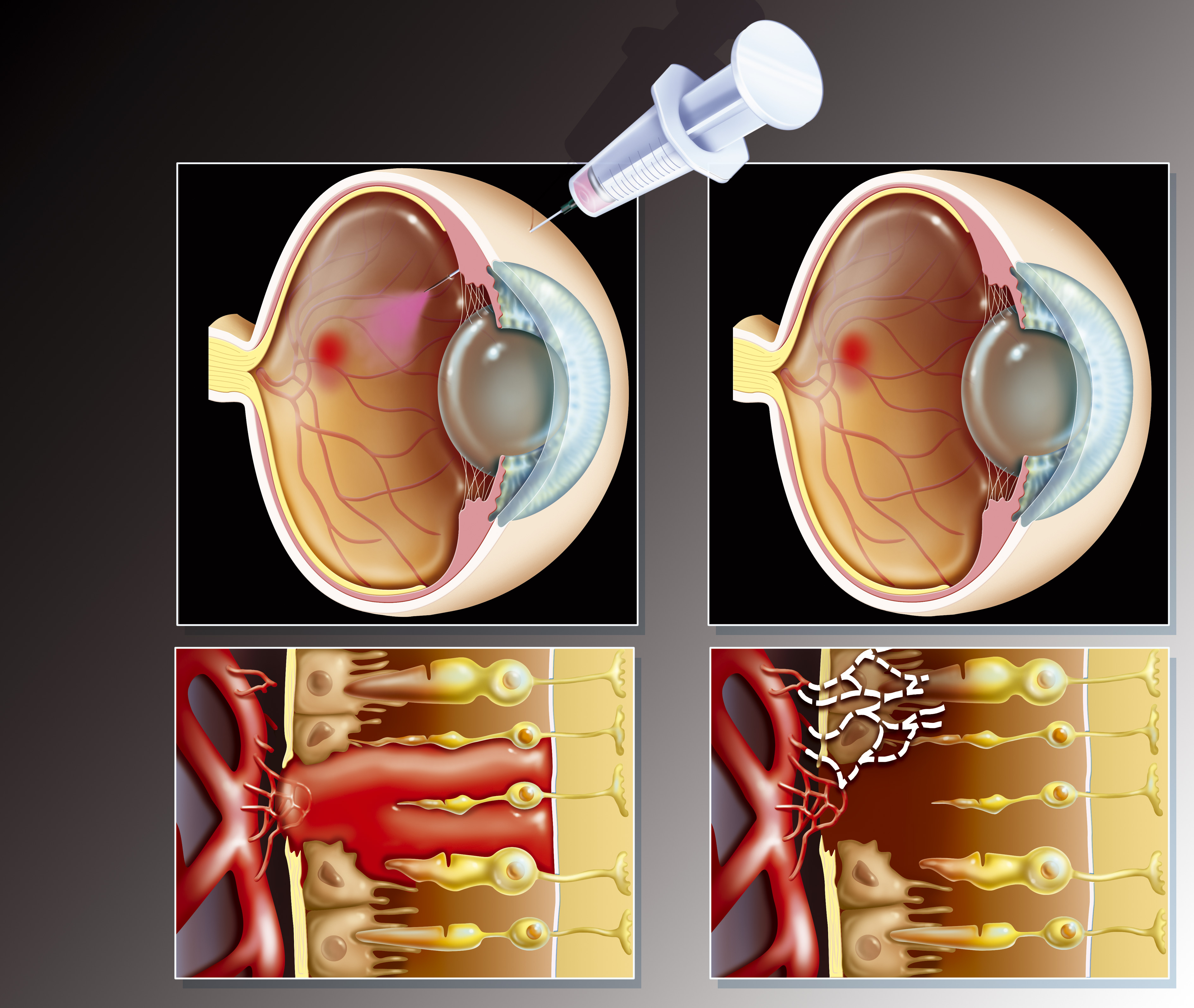
Az egyik szem génterápiás kezelésével mindkét szem látását visszaállították egy kísérletben
A klinikai vizsgálat alanyainak 78 százalékánál sikerült visszafordítani az örökölt látásromlás egy típusát, de arra még a kutatók sem számítottak, hogy a placebót kapott szemben is végbemegy a javulás.

Hamarosan magyar betegeken is tesztelhetik az egyedülálló látás-visszaállító terápiát
A Semmelweis Egyetem Szabó Arnold vezette kutatócsoportja a Svájcban dolgozó, világhírű Roska Botonddal és kutatócsoportjával karöltve olyan eljárást dolgozott ki, amely vissza tudja állítani a teljesen elhalt retina fényérzékenységét is.

Roska Botond: Olyan vakság, amin nem lehet segíteni, nem létezik
Még ha nem is ugyanolyan fokú javulást eredményezne mindenkinél, a látás-visszaállító terápia csak pénz kérdése – mondta a Qubitnek a Svájcban élő Roska Botond neurobiológus, akit több rangos orvosi díjat első magyarként érdemelt ki, a legutóbbit a múlt héten.
