Elektronmikroszkóppal térképezték föl az omikron molekulastruktúráját

A UBC kutatói a világon elsőként készítették el a koronavírus omikron variánsának molekuláris szintű strukturális elemzését – pontosabban a tüskefehérjéét. A kutatók csaknem atomi szinten elemezhették a vírus felépítését a munkához használt krio-elektronmikroszkóp segítségével.
A vizsgálat felfedte, hogy az erősen mutálódott vírusvariáns megfertőzheti az emberi sejteket, és hatékonyan kerüli meg az immunválaszt. Az eredmények nemcsak azt a kérdést helyezik új megvilágításba, hogy az omikron variáns miért terjed ilyen hatékonyan, hanem új, hatékonyabb kezelési módszerek fejlesztésének is megágyazhatnak.
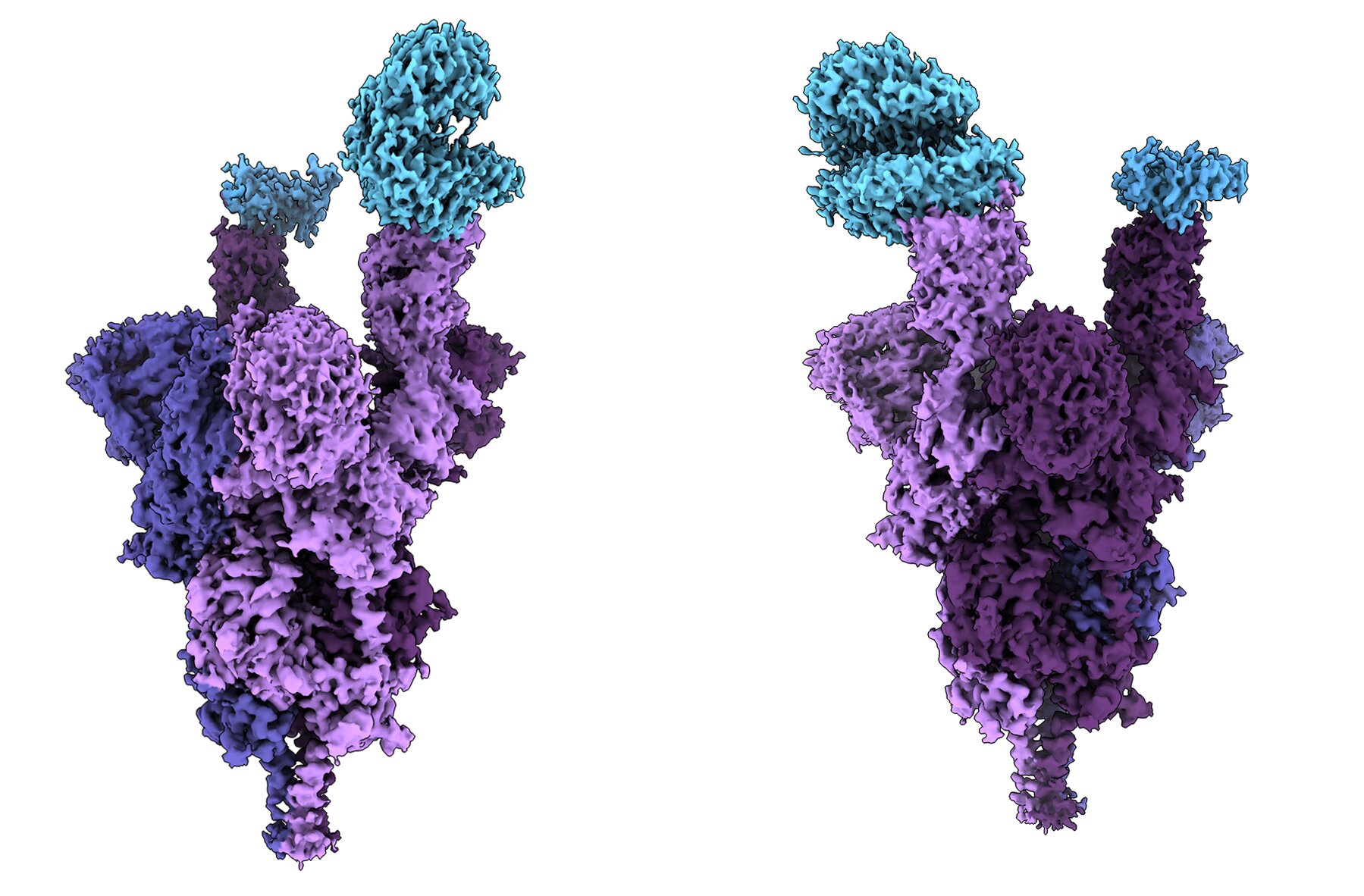
A kutatást Dr. Sriram Subramaniam, a UBC gyógyszerészeti és vegyészeti tanszékének professzora vezette. A megállapításaikat leíró tanulmányuk még szakmai felülvizsgálat alatt áll, de a preprint főbb megállapításait már szemlézte a Medicalxpress hírportál.
Temérdek tüskefehérje-mutációja van
Az omikron variánsnak meghökkentően sok, 37 tüskefehérje-mutációja van; 3-5-ször annyi, mint amennyi a korábbi variánsoknak. Ez két okból is fontos: egyrészt mert a vírus a tüskefehérjével kapcsolódik az emberi sejtekhez; másrészt mert az antitestek a tüskefehérjéhez kapcsolódva győzik le a vírust. A tüskefehérje-mutációk vélhetően nagy hatással vannak a vírus terjedésére, az immunválaszra, és a kezelési módok hatékonyságára. A kutatók szerint figyelemre méltó, hogy az omikron variáns ilyen szerteágazó és kiterjedt mutációk után is ennyire hatékonyan tud kapcsolódni az emberi sejtekhez.
Ragályosabb az első SARS-CoV-2-nél
A koronavírus számos mutációjánál, többek között az R493-nál, az S496-nál és az R498-nál is megfigyelték, hogy új hidrogénkötéseket és sóhidakat hoznak létre a tüskefehérje és az emberi sejt ACE2 nevű receptora között. Ez látszólag növeli a kötődési affinitást (azt, hogy a vírus mennyire erősen kötődik más sejtekhez), míg más mutációknál, például a K417N-nél csökken a kötődési affinitás. Az előzetes eredmények alapján az omikron variáns kötődési affinitása magasabb, mint az eredeti SARS-CoV-2 vírusé volt.
Ellenállóbb az antitestekkel szemben
A kutatók kísérletei beigazolták azt, amit a gyakorlati tapasztalat alapján eddig is sejthettünk: hogy az omikron tüskeproteinje más variánsoknál rosszabbul reagál a monoklonális antitest-kezelésekre, és mind a koronavírus-fertőzés útján szerzett, mint a védőoltás által nyújtott immunitással szemben ellenállóbb lehet.
Az oltás nyújtja a legjobb védelmet
Ez persze nem azt jelenti, hogy a védőoltás vagy a fertőzés útján szerzett immunitás nem ér semmit. Az eredmények alapján az oltás hatékonyabban védhet meg az omikrontól, mint a fertőzésen átesett betegek immunválasza. Vagyis – írták a kutatók – ezek alapján arra következtethetünk, hogy még mindig a vakcina nyújtja a leghatékonyabb védelmet az omikron variánssal szemben.
A mutációk gyorsíthatták a terjedését
A kutatók szerint a tüskefehérje-mutációk sajátosságai nagy mértékben hozzájárulhattak ahhoz, hogy az omikron variáns a gyors terjedésének köszönhetően mára a legdominánsabb lett az összes SARS-CoV-2 variáns közül.
Jöhetnek a hatékonyabb kezelési módok
A tüskefehérje molekulastruktúrájának ismerete vélhetően megnyitja majd az utat a hatékonyabb kezelési eljárások fejlesztése előtt. Ehhez viszont meg kell értenünk, hogy a vírus hogyan kapcsolódik az emberi sejtekhez, és hogyan fertőzi meg őket. A kutatók szerint fontos megismerni azt a mechanizmust, ami a tüskefehérje és az antitestek kötődését szabályozza. Ennek a feltárása új kezelési eljárások kifejlesztésében segíthet, amiket variánstól függetlenül, egységesen lehet alkalmazni.
Kapcsolódó cikkek a Qubiten:
Elképesztően gyorsan képes terjedni az omikron, de az AstraZeneca, a Moderna és a Pfizer felveszi vele a harcot
A két vakcinadózis továbbra is jól védhet a súlyos megbetegedés ellen, de fontos a harmadik oltás. A Janssen, a Sinopharm és a Szputnyik egy átfogó nemzetközi kutatás szerint nem sokat ér az omikron ellen, bár a Gamelaja Intézet szerint az orosz vakcinával minden rendben.

Az eddigi adatok alapján enyhébb tüneteket okoz, de fertőzőbb a koronavírus új variánsa
A korai kórházi adatok alapján úgy tűnik, hogy kevesebb omikronos beteg szorul gépi lélegeztetésre, mint deltával fertőzött, de a kutatók arra figyelmeztetnek, hogy az új variáns gyorsabban terjed, mint az eddigiek, ezért egy új hullám még így is túlterhelheti a kórházakat.
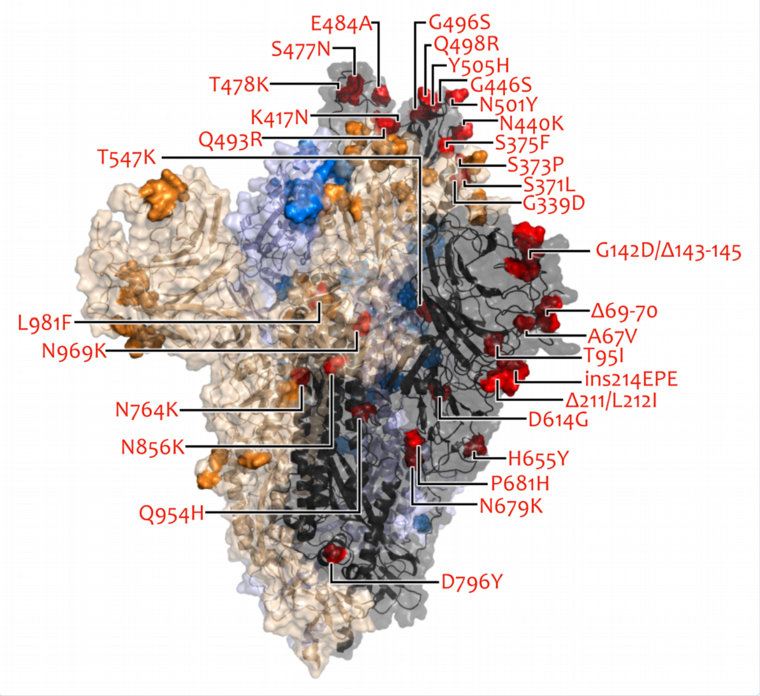
Látványosan sok aggasztó mutációval rendelkezik az omikron, de még nem tudni, milyen lesz az együttes hatásuk
Elképzelhető, hogy az új vírusvariáns egy vagy több immunhiányos betegben, krónikus koronavírus-fertőzés során alakult ki, de az is lehet, hogy újabb zoonózis eredménye, vagyis az emberről egy ismeretlen állatfajra került, és onnan jutott vissza az emberi populációba. Az oltások valószínűleg továbbra is védenek a súlyos betegség ellen, és feltehető, hogy a gyógyszerek hatásossága sem csökken.