Minden, amit a tudomány eddig felderített a koronavírusról

A 2019 végén a kínai Vuhanban felbukkant új koronavírus eddig közel 110 ezer embert fertőzött meg, és több mint 3600 áldozatot követelt. Bár nem látszik még a járvány vége, a tudományos közösség példátlan erőfeszítésének köszönhetően sikerült gyorsan feltárni a vírus fontosabb jellemzőit, megindult az oltások kifejlesztése, és zajlik a fertőzés ellen potenciálisan hatásos gyógyszerek tesztelése.
Január végi és február eleji összefoglaló cikkeinkben részletesen írtunk a vírus biológiai és genetikai hátteréről, valamint azokról a gyógyszerekről, amelyek szóba jöhetnek a betegség kezelésekor. Itt a vírussal kapcsolatos alapvető információkat és az azóta megjelent tudományos fejleményeket tekintjük át.
A SARS-CoV-2-nak elnevezett új koronavírus (korábbi ideiglenes nevén: 2019-nCoV) a beta-koronavírusok közé tartozik, amelyek burokkal rendelkező, úgynevezett pozitív-szálú RNS-vírusok. A pozitív szálúság arra utal, hogy a vírus egyszálú RNS-örökítőanyaga a sejtbe kerülést követően a sejt fehérjeszintetizáló gépezetén szinte azonnal le tud fordítódni az általa kódolt vírusfehérjékké. A beta-koronavírusok csoportján belül a SARS-CoV-2 egy B-típusú, a Sarbecovirus vonalhoz tartozó kórokozó - a SARS-al és számtalan denevérekben jelen lévő koronavírussal együtt. A koronavírusok a felszínükön lévő tüskék által létrehozott, napkoronára emlékeztető elektronmikroszkópos megjelenésük után kapták nevüket. Ezeket a tüskéket a vírus S-fehérjéje hozza létre, amely a sejt receptoraihoz kapcsolódva bejuttatja a vírust az emberi sejtbe.
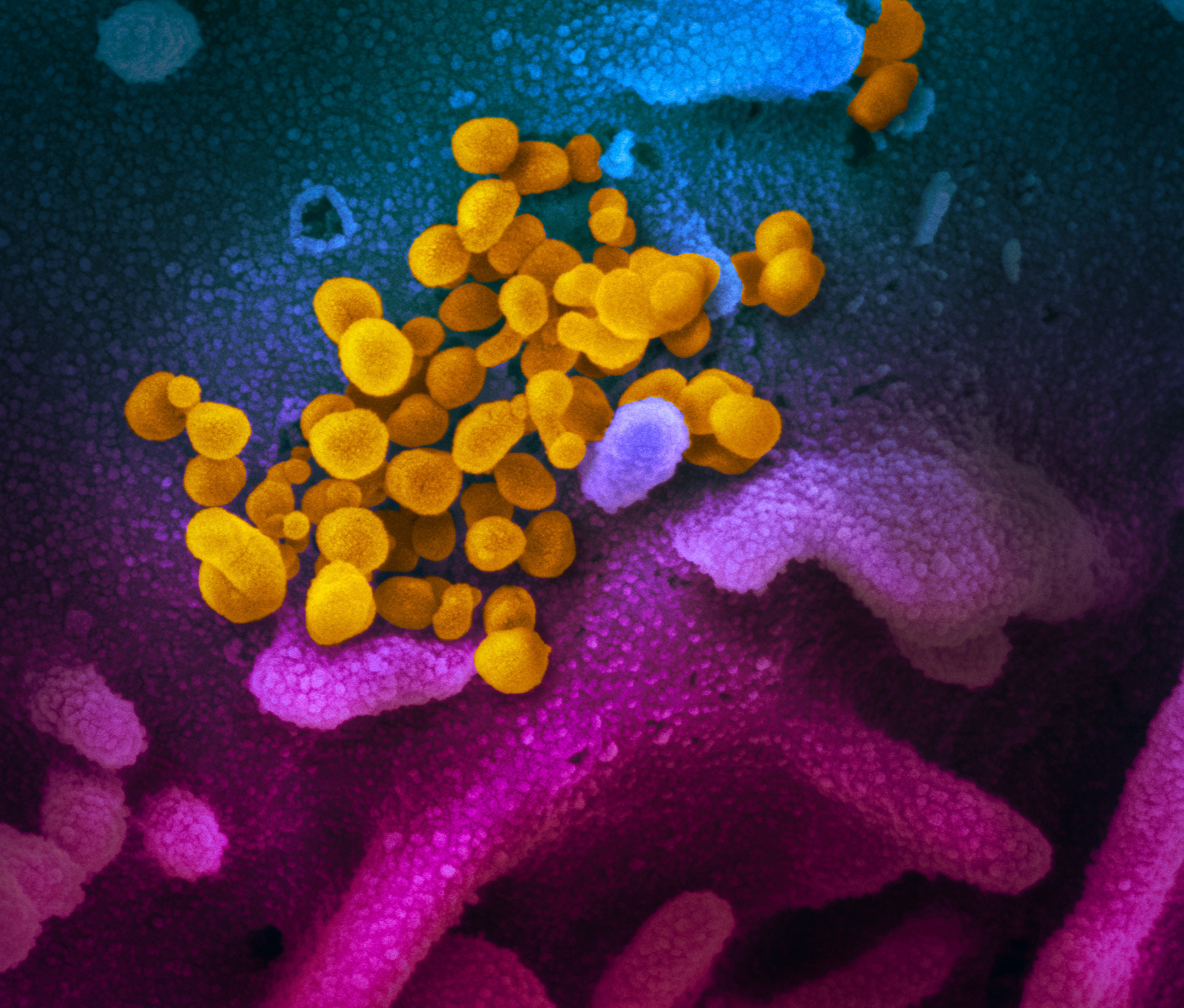
A SARS-COV-2 vírus okozza a COVID-19 betegséget, amely az esetek túlnyomó többségében enyhe, influenzához hasonló tüneteket eredményez. Súlyosabb esetben azonban vírusos tüdőgyulladás és más komplikációk alakulhatnak ki, ami a megfertőzöttek nagyjából 1-2 százaléka esetében halálos kimenetelűvé teszi a fertőzést - főleg idősek vagy egyéb módon veszélyeztetett betegek esetén. Bár a COVID-19 néhány tünetében emlékeztet az influenzára, az influenzavírusok és a koronavírusok egymástól nagyon távoli és nagyon különböző RNS-vírusok – egyszerűbben fogalmazva a koronavírusoknak semmi köze az influenzavírusokhoz.
Megvan, hogyan jut be a vírus a sejtbe
A SARS-CoV-2 közel 29 900 bázispárból álló genomjából már több mint 230 érhető el, amelyeket a szakemberek a világ majdnem minden pontjáról gyűjtöttek, és elérhetővé tettek a GISAID vírusadatbázisban. A vírus genomját a kutatók egy szekvenálásnak nevezett módszerrel határozzák meg, amely feltárja a nukleotid-bázisok sorrendjét a vírus RNS örökítőanyagában, és egy digitális kódot eredményez. A vírus RNS-éből kiderül, hogy milyen fehérjék építik fel a kórokozót, ez pedig segít megérteni annak működését, ezzel lehetővé téve hatásos ellenszerek vagy oltások kifejlesztését. A vírusgenomok emellett feltárják a járvány eredetét, alakulását és a kórokozó evolúcióját. Az új genetikai módszerek emellett tovább segítik a vírus funkcionális elemzését.
Az január vége óta ismert, hogy az új koronavírus S-fehérjének egy alegysége (RBD, receptorkötő domén) a korábbi SARS-vírushoz hasonlóan az emberi sejtek felszínén levő ACE-2 receptorhoz kapcsolódik. Ennek segítségével jut be a sejtbe, ahol aztán a sejt genetikai gépezetének eltérítésével elkezdi megsokszorozni magát. Február elejére kiderült, hogy egy másik, a sejtmembránban lévő enzimfehérje, a TMPRSS2 is szükséges a vírus sejtbe való bejutásához.
Egy március 4-én a Science folyóiratban megjelent tanulmány ennél is tovább visz annak megértésében, hogy miként kerül be a vírus a sejtekbe. A kutatók ugyanis feltárták az ACE-2 receptor és a B(0)AT1 aminosav-transzportfehérje által alkotott komplexum, illetve a vírus ehhez kapcsolódó S-kötőfehérje alegységének (RBD, receptorkötő domén) szerkezetét. A szerkezet nagy felbontású vizsgálata elárulta a kutatóknak, hogy két S-fehérje trimer köt egyszerre egy ACE-2 dimerhez. Mindez pedig lehetővé teheti akár az ACE-2-höz, akár a vírus S-fehérjéjéhez jól kötő hatóanyagok létrehozását. Egy március 5-én, a Cell folyóiratban közölt tanulmány alapján úgy tűnik, már van is egy ilyen hatóanyag. A szerzők egy klinikai használatra elfogadott TMPRSS2 enzim-blokkolót teszteltek, amely sikeresen blokkolta a vírus sejtbe jutását. A kutatás annyiban limitált volt, hogy a kutatók egy koronavírus S-fehérjét hordozó, kísérletekben gyakran használt vírusmodellt használtak vizsgálataikhoz.
Mint arról már írtunk, a SARS-CoV-2 legközelebbi rokona egy 2013-ban egy patkósdenevérből (Rhinolophus affinis) izolált denevér-koronavírus, a BatCoV RaTG13, amellyel genetikailag 96 százalékos egyezést mutat. Emiatt lényegében biztos, hogy a SARS-CoV-2 eredeti hordozói denevérek; a köztes faj azonban, amelyről végül a kórokozó az emberre átugrott, továbbra is ismeretlen. Ahogy arról Kun Ádám már írt a Qubit-on, a tobzoskák köztes fajként való megállapítása alapvetően egy félreértésen alapul – egyértelmű genetikai bizonyíték legalábbis biztosan nincs rá. A genetikai adatok elemzése alapján ugyanakkor továbbra is az tűnik valószínűnek, hogy a járvány a vuhani élőállatpiacról indult el.
Folyamatosan követhető a vírus evolúciója
A vírus RNS-örökítőanyagának sejtekben történő megsokszorozódásakor a mechanizmus néha hibázik, ami bázisváltozáshoz vagy mutáció kialakulásához vezethet a vírus genomjában. Az így létrejött változások többsége az esetek nagy részében vagy nem befolyásolja a vírus működését (neutrális mutáció), vagy hátrányt okoz neki.
Nemrég nagy médiavisszhangot váltott ki egy a National Science Review folyóiratban megjelent, kínai kutatók által írt, a vírus evolúcióját elemző tanulmány. Fő állítása azonban, miszerint két, különböző veszélyességű és terjedési képességű vírustörzs alakult volna ki, nem megalapozott. Független szakemberek a tanulmány visszavonását követelik, mert a benne megfogalmazott állítások félreértéseken, a rendelkezésre álló adatok túlértelmezésén, valamint módszertani limitációkon alapulnak.
A tudomány jelenlegi állása szerint a SARS-CoV-2 egyetlen vírustörzset alkot, és a genomikai adatokból emellett az is világos, hogy viszonylag lassan változik. A vírusok evolúciójának követésére létrehozott Nextstrain bioinformatikai szoftver és weboldal segítségével folyamatosan figyelhető a SARS-CoV-2 evolúciója, mégpedig azáltal, hogy a szoftver a SARS-CoV-2 elérhető genomjaiból egy leszármazási rokonságot kimutató, úgynevezett filogenetikai törzsfát hoz létre a vírus genetikai kódjának imént tárgyalt mutációiból eredő különbség alapján.
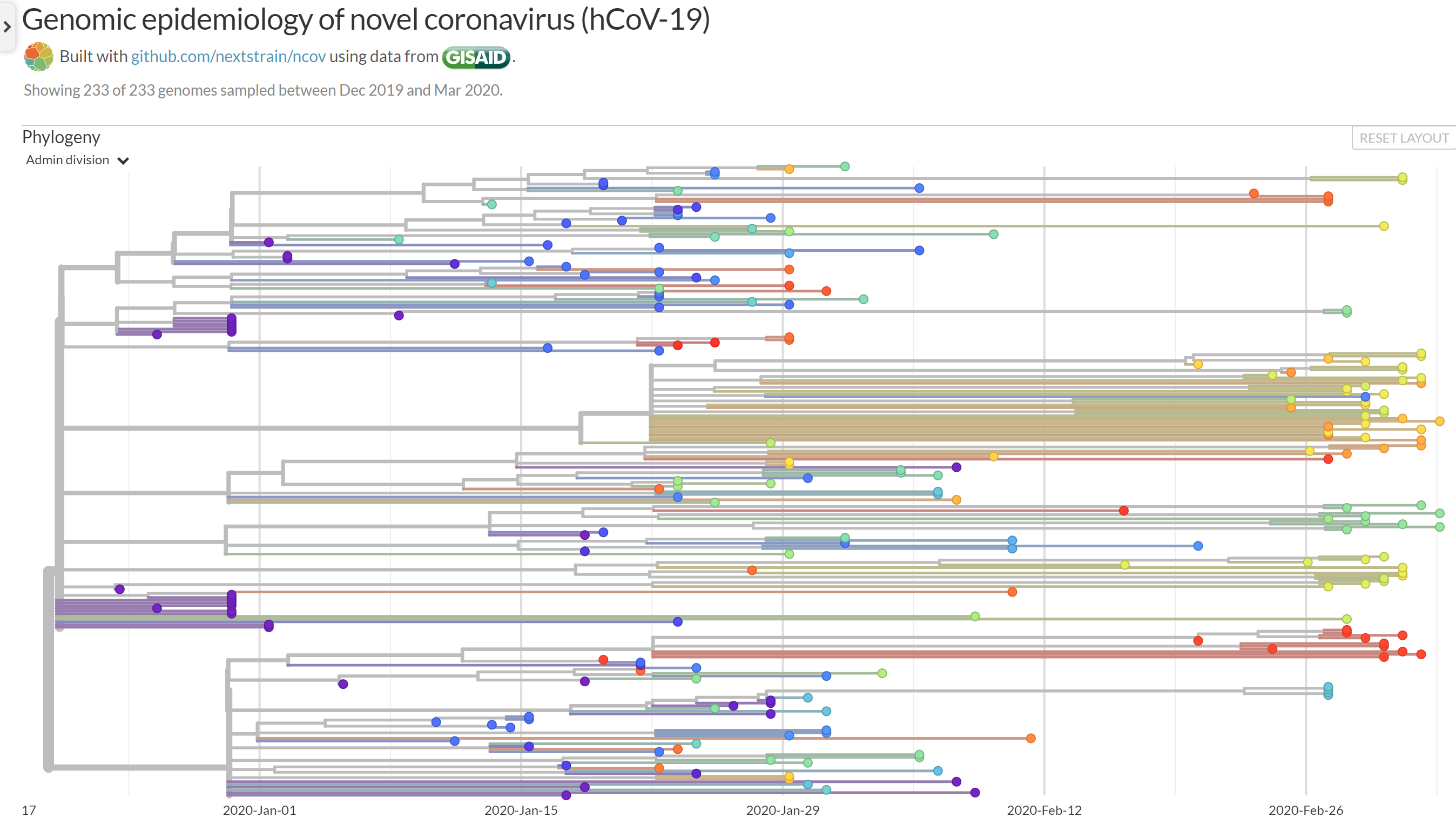
A Nexstrain mögött álló szakemberek viszonylag közérthető legújabb genomikai analízise itt olvasható.
A nyugati világban példátlan járványügyi intézkedések Olaszországban
Az Európai Járványügyi és Betegségmegelőzési Központ (ECDC) legfrissebb elemzésealapján a SARS-CoV-2 alap szaporodási rátája (R0) 2 és 3 között van, valószínűleg 2,2 körül. Ez annyit jelent, hogy egy fertőzött ember átlagosan 2,2 másikat fertőzhet meg. Fontos azonban, hogy az R0 nem állandó érték: a higiéniára való jobb odafigyelés vagy a járványügyi intézkedések radikálisan csökkenthetik értéket, vagyis a fertőzés terjedését.
A járvány által jelenleg leginkább sújtott európai ország Olaszország, ahol március 8-án nyugati demokráciákban eddig példátlan karanténintézkedéseket vezettek be. Ezek értelmében közel 16 millió, Lombardiában és 14 más régióban élő ember mozgását korlátozták, és ők csak speciális engedéllyel hagyhatják el lakóhelyüket. A területeken belül további, a járvány terjedését mérséklő intézkedéseket léptetnek életbe az olasz hatóságok.
A COVID-19 megbetegedés halálozási aránya 1 százalék körül, vagy talán az alatt lehet. Az Egyesült Királyság kormányának vezető egészségügyi tanácsadója, Chris Whitty epidemiológus Boris Johnson brit miniszterelnök múlt hétfői sajtótájékoztatóján úgy nyilatkozott, hogy a megbetegedés számításaik szerint 1 százalék körüli halálozási aránnyal jár. Ez egybevág az Imperial College London kutatóinak becslésével. Az ENSZ Egészségügyi Világszervezete, a WHO kínai feltáró misszióját vezető Bruce Aylward a New York Timesnak március elején nyilatkozva 1-2 százalék közé becsülte a valós halálozási arányt.
Az Európai Betegségmegelőzési és Járványvédelmi Központ, az ECDC szerint továbbá nincs komoly bizonyíték arra, hogy a fertőzés tünetmentes állapotban is terjedne. A vírus inkubációs periódusát 5-6 napban állapítják meg, hozzátéve, hogy ez extrém esetben 14 nap is lehet.
Korábban Müller Viktor, az ELTE Biológiai Intézetének vírusok számítógépes modellezésével foglalkozó kutatója a Qubitnek nyilatkozva felvetette, hogy a SARS-CoV-2 is szezonális vírus lehet, ami lelassíthatja a járvány terjedését a nyár közeledtével. A WHO azonban nem lát erre eddig bizonyítékot. Ennek ellenére a szezonalitás lehetőségét svájci és svéd egyetemeken, illetve kutatóintézetekben dolgozó kutatók egy friss tanulmányukban modellezték. Vizsgálatukat arra a feltételezésre alapozták, hogy a SARS-CoV-2 más, emberben enyhe megfázást okozó koronavírusokhoz hasonlóan viselkedhet. Bár konklúziójukban világossá teszik, hogy a nyár közeledtének lehet valamekkora negatív hatása a jelenlegi járvány terjedésére, szerintük ez hamis biztonságérzetet is kelthet, hogy aztán az év végén, a tél közeledtél ismét meginduljon a terjedés.
12-18 hónap múlva lehet oltás
A SARS-COV-2 elleni védekezés legjobb módját egy hatásos oltás jelentené. Ennek kifejlesztése, legyártása és szétosztása azonban akár 12-18 hónapot is igénybe vehet – legalábbis egy sajtótájékoztatón így nyilatkozott Anthony Fauci, az Egyesült Államok fertőző betegségekkel foglalkozó intézetének (National Institute of Allergy and Infectious Diseases, NIAID) vezetője.
Egy a bioRxiv, folyóiratban történő publikálás előtt használt szerverre február végén feltöltött tanulmányban kutatók egy SARS-vírus ellen kifejlesztett oltás teszteléséről számolnak be. A rézuszmajmokban kipróbált rekombináns, azaz a vírus fehérjedarabkáival immunválaszt generáló oltás viszonylag hatásosnak bizonyult, ugyanakkor mindez igen kezdeti lépést jelent csak, főleg, hogy a SARS és a SARS-CoV-2 vírusok között lényeges különbségek vannak.
Egy másik, kifejezetten a SARS-CoV-2 ellen kifejlesztett kísérleti oltóanyag talán már érdekesebb. Ez a Moderna amerikai gyógyszercég által az NIAID intézettel együtt, a SARS-CoV-2 genomjából származó információk segítségével elkészített oltóanyag. A tervek szerint ennek korai, első fázisú klinikai vizsgálatait az NIAID már áprilisban megkezdheti. Ennek a minimum három hónapig tartó folyamatnak a célja, hogy eldöntsék, biztonságos-e az oltóanyag emberi használatra. Az oltás hatásosságát firtató tesztek további 6-8 hónapig tarthatnak. Ugyanakkor, mint arra a Wall Street Journal felhívja a figyelmet, a Modernának eddig egyetlen hasonló módszerekkel tervezett oltást sem sikerült még forgalomba hoznia, és ez mindenképpen óvatosságra int a kezdeti stádiumban lévő, kísérleti oltóanyaggal kapcsolatban.
Hamarosan kiderül, hatásosak-e a vírus ellen bevetett gyógyszerek
Korábbi cikkünkben részletesen foglalkoztunk a vírusok ellen alkalmazott antivirális gyógyszerekkel és működési módjaikkal. A SARS-CoV-2 vírus ellen több már engedélyezett vagy kísérleti stádiumban lévő antivirális gyógyszer merült fel potenciálisan hatásos kezelési lehetőségként.
A talán legígéretesebb ezek közül a Gilead gyógyszercég kísérleti antivirális gyógyszere, a Remdesivir. Ez, az eredetileg az Ebola-vírus ellen kifejlesztett hatóanyag az RNS-nukleozid-analóg antivirális gyógyszerek közé tartozik. Ezek meggátolják a vírus RNS-ének szintézisét azáltal, hogy a folyamat során „alapanyagként” beépülnek a növekvő nukleinsavláncba, majd blokkolják a szintézishez szükséges RNS-polimeráz enzimet.
A korábbi tudományos kísérletek alapján potenciálisan hatásos Remdesivirt még január végén alkalmazták egy amerikai páciens kezelésére. Február elején pedig a COVID-19 gyógyításában mutatott hattesztelésére Kínában kezdeti klinikai vizsgálatot indítottak a Gilead együttműködésével.
Közben egy február közepén, a PNAS folyóiratban megjelent tanulmány eredményesnek találta a Remdesivirt a MERS-koronavírus-fertőzés ellen, legalábbis a rézuszmajmokban, ami egybevág korábbi kutatások eredményeivel. A PNAS-ban megjelent tanulmány szerzői kísérleteik alapján elképzelhetőnek tartják, hogy a Remdesivir a COVID-19 megbetegedés kezelésében is szerepet játszhat.
Potenciálisan a SARS-CoV-2 ellen bevethető gyógyszerként felmerültek HIV ellen alkalmazott LPV/r proteáz blokkolók (melyek gátolják a vírus sejtekben való szaporodását a vírus felépítéséhez nélkülözhetetlen érett fehérjék keletkezésének megállításával), illetve más hatóanyagok is. Az egyik ilyen a Galidesivir, amely a Remdesivirhez hasonlóan egy nukleozid-analóg antivirális hatóanyag, ami korábbi alapkísérletekben hatásosnak bizonyult más koronavírusok ellen.
A legfontosabb fejlemény a potenciális gyógyszerek ügyében, hogy a WHO szerint március közepe után érkezhetnek meg a kínai klinikai vizsgálatok eredményei. Ezekből kiderül majd, hogy hatásos-e valamelyik gyógyszer a COVID-19 megbetegedés kezelésére. A klinikai tesztek a Remdesivir mellett az LPV/r proteáz blokkolókat is érintik.
Szintén klinikai tesztek alatt áll a malária és autoimmun betegségek elleni klorokin nevű gyógyszer is, amely egy február eleji tanulmány szerint potenciálisan meggátolhatja a SARS-COV-2 vírusok sejtbe jutását és működését. Emellett az immunválaszt enyhítő hatása paradox módon szintén javíthatna a legbetegebb páciensek állapotán. A klorokin további előnye az lenne, hogy széles körben, olcsón elérhető, régi gyógyszerről van szó. De talán pont ezek miatt is még nagyobb óvatossággal kell kezelni addig, amíg nincsenek meg a klinikai vizsgálatok eredményei.
Fontos továbbá hangsúlyozni, hogy akkor sincs minden veszve a potenciális gyógyszeres kezelést tekintve, ha a kezdeti klinikai tesztek nem hoznak eredményt. Jó példa erre a március 5-én a Cellben közölt tanulmány, aminek alapján a Camostat fehérjebontóenzim-blokkoló újabb kezelési lehetőséget biztosíthat. Az igazi kérdés az, hogy a sok elvileg működőképes hatóanyag közül melyik használható majd végül gyógyszerként.
Kapcsolódó cikkek a Qubiten:

Tobzoskától, denevértől, sőt mind a kettőtől is származhat a rettegett koronavírus
A SARS-CoV-2 névre keresztelt, lassan tényleg az egész világra kiterjedő járványt okozó koronavírus eredetét még mindig homály fedi.

A koronavírust nem azért nehéz megállítani, mert különösen agresszív, hanem azért, mert nem az
Lassan nincs olyan európai ország, ahol ne jelent volna meg hivatalosan is a koronavírus, de Magyarország határain belül még nem azonosítottak fertőzöttet. Az aggodalom jeleit viszont annál inkább.

Ha szerencsénk van, nyáron lelassulhat az új koronavírus terjedése
Ha ebből lesz is világjárvány, Európába akkor ér el az első hullám, amikor már beköszöntött a tavasz vagy a nyár, és ez óriási szerencse lehet, mondta Müller Viktor, az ELTE TTK elméleti biológus kutatója, aki a Magyar Tudományos Akadémián tartott előadást az új koronavírus által okozott járványról.

A koronavírus már a gazdaságot is megfertőzte
Tovább terjed a koronavírus, ezt pedig azokon a területeken is megérzik, ahol még nem történtek fertőzések: a gazdaság is kezd köhécselni, a Kínából érkező árucikkek hiányát pedig egyre többen érzik meg világszerte.

Jankovics István virológus: Az új koronavírus alig fertőzőbb, mint egy átlagos influenza
A Kínából világ körüli útra indult koronavírus egyelőre csak az idősek és a krónikus betegek közül szed halálos áldozatokat. A karantén akár kontraproduktívan is hathat, de a gyakori kézmosás javasolt – mondta Jankovics István virológus-mikrobiológus, aki korábban a WHO hazai laboratóriumában volt vezető főorvos.
Bevetették az első gyógyszereket a koronavírus ellen
Egy Remdesivirrel kezelt beteg tünetmentessé vált, bár ez még nem bizonyítja, hogy a gyógyszer minden esetben hatékony az új vírus ellen. A 2019-nCoV a szakértők által megjósolt módon megjelent európai országokban is, de további itteni terjedésére az Európai Járványügyi Hivatal szerint kevés esély van.

Hibás volt a tanulmány, amely szerint a koronavírus tünetmentesen is terjedhet emberről emberre
Az egészségesnek látszó kínai nő, aki német üzleti partnereit fertőzte meg, valójában már Németországban sem érezte jól magát, és paracetamolt szedett. Ez későn derült ki, így született a világsajtót bejáró téves tudományos eredmény.
Kapcsolódó cikkek




