Már az év vége előtt megjelenhetnek az első engedélyezett koronavírus-vakcinák

A történelem során számos járvánnyal és betegséggel megküzdött már az emberiség, de olyan valószínűleg még egyszer sem fordult elő, hogy egy védőoltás fejlesztésének minden apró mozzanatát olyan mértékben követhessék az érdeklődők, mint a COVID-19 esetében. Mivel a globális koronavírus-világjárványnak csak egy hatékony vakcina tud véget vetni, a világ messiásként várja annak megjelenését.
Mielőtt egy ilyen oltás bárki számára elérhetővé válhat, a hatóanyagoknak a labortesztek után klinikai vizsgálatokon is túl kell esniük, és bár a járvány alatt sosem látott mértékben felgyorsították az engedélyezési folyamatokat, több mint fél év elteltével még a legígéretesebb vakcinajelöltek is csak most lépnek a 3. klinikai fázisba. Ebben a szakaszban, ahogy a vakcinakisokosunkban is írtuk, egy nagyobb létszámú betegcsoporton vizsgálják a készítmény biztonságos alkalmazhatóságát, a hatásosságot, követik az esetleges mellékhatásokat, és összehasonlító vizsgálatokat végeznek más készítményekkel.
Az Egészségügyi Világszervezet (WHO) legfrissebb összesítése szerint jelenleg 25 oltóanyag áll klinikai tesztelés alatt, míg további 141 a preklinikai fázisban jár, tehát embereken még nem próbálták ki.
Eredményeket eddig értelemszerűen csak az első (néhány önkéntesen elvégzett teszt) és a második (kis létszámú csoporton végzett teszt) klinikai fázisról tudtak felmutatni, és ezek alapján úgy tűnik, van ok a reményre: az elmúlt hetekben több vakcinafejlesztő cég is közölt vizsgálati eredményeket, és mindegyiküknél sikerült a SARS-CoV-2-éhez hasonló immunválaszt kiváltani, minimális mellékhatások kíséretében – leginkább izomfájdalmat, lázat és fejfájást jegyeztek fel a kutatók, de ezek általában jellemzők a legtöbb védőoltásra.
Bár a Moderna, a Pfizer, az AstraZeneca, a Sinopharm és a CanSino nem ugyanazzal a technológiával dolgozik, egyvalami közös az öt cég vakcinajelöltjében: olyan semlegesítő antitestek termelését indítják be a szervezetben, amelyek a fertőző vírusrészecskékkel szemben védik a sejteket.
Moderna / NIAID
Most talán Moderna erőfeszítései vannak leginkább előtérben, az amerikai cég ugyanis az ország koronaguruja, Anthony Fauci által vezetett Nemzeti Allergia és Fertőző Betegségek Intézetével (NIAID) közösen fejleszti az oltóanyagot.
A cég márciusban elsőként tesztelhette embereken a vakcinajelöltjét: a klinikai vizsgálatra jelentkező 45 felnőtt korú (18 és 55 év közötti) alanyt az oltóanyag dózisa szerint három csoportba osztották, majd 28 nap eltéréssel kétszer beoltották őket. Az első klinikai fázis eredményei szerint minden páciensnél sikerült kiváltani a semlegesítő antitestek termelését, ráadásul a későbbi fázisokba továbbvitt 100 mikrogrammos csoport tagjainál erősebb antitesttermelést figyeltek meg, mint a felépült covidos betegeknél.
A mellékhatások az alanyok többségénél enyhék voltak, egyedül a legmagasabb dózissal, 250 mikrogrammnyi hatóanyaggal tesztelt csoportban akadt három olyan páciens, aki súlyos mellékhatást tapasztalt. A második fázisról, amelyben már 18 év alattiakat és 55 év fölöttieket is vizsgáltak, egyelőre nem közöltek eredményeket, a tesztelés harmadik szakaszát pedig július 27-én kezdték meg, összesen körülbelül 30 ezer önkéntes részvételével.

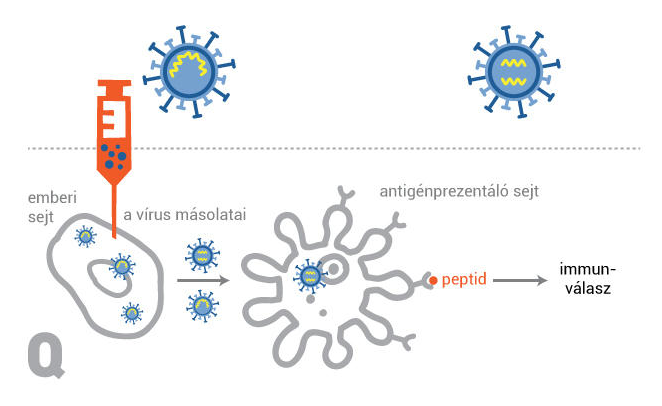
A Moderna vakcinája úgynevezett hírvivő RNS-ek (vagy mRNS-ek) felhasználásával fejti ki hatását. A sejtek ezeknek a molekuláknak a segítségével építik fel a fehérjéket, jelen esetben a SARS-CoV-2 koronavírus tüskéjét (vagy S-fehérjéjét), amellyel a vírus rákapcsolódik a sejtekre, elindítva a fertőzési folyamatot. Minél előbb ismeri fel a szervezet ezt a fehérjét, annál gyorsabban tud rá immunválaszt adni, vagyis mire egy ilyen védőoltást kapott személyt megfertőzne a koronavírus, az már nem tudna nagyon elburjánzani a szervezetében, így a betegség is elkerülhetővé válna.
A cég vasárnap jelentette be, hogy az áprilisban kapott 483 millió dolláros állami támogatást újabb 472 millióval egészítette ki az orvosbiológiai kutatás-fejlesztést támogató kormányszerv, a BARDA, így közel egymilliárd dollárnyi állami pénzből gazdálkodhat csak ebben a projektben. „Az első fázis eredményei alapján úgy hisszük, hogy az mRNS-vakcinánk segíthet a COVID-19-világjárvány leküzdésében és a jövőbeli fertőzések megelőzésében” – idézi a közlemény a Moderna vezérigazgatóját, Stephane Bancelt. A cég úgy számol, hogy évente legalább 500 millió, de lehetőség szerint akár 1 milliárd dózist le tud majd szállítani 2021-től kezdődően.
AstraZeneca / Oxfordi Egyetem
Az AstraZeneca története azért lóg ki a többi közül, mert a brit-svéd cég viszonylag későn, április 30-án jelentette be, hogy összeáll az Oxfordi Egyetemmel, és közösen fejlesztenek vakcinát, miután az egyetem kutatói már korábban elkezdték embereken tesztelni a saját COVID-oltóanyagukat.
Az együttes erővel kifejlesztett ChAdOx1 nevű vakcina hatóanyagát egy csimpánzoknál náthát okozó adenovírus módosításával állították elő. A klinikai vizsgálat második fázisának eredményeit a Lancet folyóiratban tették közzé a kutatók: a kísérletben 533 résztvevő egy dózist, míg tíz másik alany két dózist kapott az oltásból, majd az ő eredményeiket egy 534 fős kontrollcsoporttal is összevetették. Az önkéntesek itt is 18 és 55 év közöttiek voltak.
Az oltás után 28 nappal az alanyok 91 százalékánál figyelték meg a semlegesítő antitestek termelését egy megengedőbb mérce szerint, míg a szigorúbb elemzés 37 százalékban állapította meg azok arányát, akiknél a vírus semlegesítésére alkalmas antitestek kialakultak. A két dózisban beoltott alanyok mindegyikénél a szigorúbb mérce szerint is működött a vakcina. Az oxfordi kutatók szerint az immunválasz működésében központi szerepet játszó T-sejtek száma is nőtt az alanyoknál – az oltás után két héttel érte el a csúcsot a T-sejtek szintje.
Az 5-12 év közötti fiatalok, valamint az 56-69 közöttiek és 70 fölöttiek bevonásával közel 50 ezer önkéntest számláló következő, kevert (helyszíntől függően 2. vagy 3.) fázist Angliában, Brazíliában és Dél-Afrikában már megkezdték, de hamarosan az Egyesült Államokban is sort kerítenek rá.
A kutatók szerint októberben már rendelkezésre állhatnak olyan kísérleti vakcinák, amiket vészhelyzet esetén be lehet vetni, míg az AstraZeneca szerint engedélyezés után akár kétmilliárd dózist is le tudnak gyártani. A cég eddig 1,2 milliárd dollárt kapott az amerikai kormánytól, a vakcinafejlesztés felgyorsításának elősegítésére létrehozott Operation Warp Speed nevű programban. Ezzel egyébként még mindig csak a második helyen áll a támogatott gyógyszeripari cégek sorában, a klinikai vizsgálatokról egyelőre semmilyen adatot nem szolgáltató Novavax 1,6 milliárdot kapott a program költségvetéséből.
Pfizer / BioNTech / Fosun Pharma
Az amerikai-német-kínai együttműködésben a Modernához hasonlóan RNS-alapú vakcinákat fejlesztenek, ráadásul négy különböző típusút, és júliusban két klinikai vizsgálat eredményeiről is beszámoltak. Míg a Németországban végzett vizsgálat még az első klinikai fázisban járt, az amerikai tesztről készült jelentés már a második fázis tapasztalatait írja le: az alanyok két dózist kaptak két különböző erősségű oltóanyagból, és az oltásokat követően a covidos betegekhez képest 1,8–2,8-szoros mennyiségben mutattak ki a szervezetükben semlegesítő antitesteket, miközben a T-sejtek száma is nőtt.
A cégek július végén terveznek belevágni a klinikai vizsgálatok harmadik fázisába, 30 ezer önkéntes tesztalannyal. Bár az Operation Warp Speed büdzséjéből az ő támogatásukra nem futotta, nem kerültek túl nagy üzleti hátrányba: július 22-én 1,95 milliárd dolláros szerződést kötöttek az amerikai kormánnyal, amelynek értelmében decemberig százmillió vakcinát kell legyártaniuk és szállítaniuk, valamint egy opció szerint további 500 millió dózisra igényt tarthat a kormány. A Pfizer számításai szerint 2021 végéig 1,3 milliárd adag oltóanyagot tudnak legyártani.
A kínai vonal
Mivel Kína már azelőtt rengeteg adattal rendelkezett a vírusról, hogy az elindult volna világ körüli útjára, a kínai gyógyszeripari és biotechnológiai cégek lépéselőnyből indultak nyugati versenytársaikhoz képest a vakcinafejlesztés területén is. Ezt a területet jelenleg három cég uralja az országban: a tiencsini CanSino Biologics, a pekingi Sinovac Biotech és az állami Sinopharm, másik nevén a Kínai Nemzeti Farmakológiai Csoport.

A CanSinónál az AstraZenecához hasonlóan egy nem replikálódó vírusvektoron alapuló vakcinát tesztelnek, vagyis a koronavírus tüskéjét kódoló géneket egy ártalmatlan, korlátozott fertőzőképességű adenovírussal juttatják a szervezetbe, hogy a sejtek maguk készíthessék elő az immunválaszt. A második klinikai fázis azonban a nyugati próbálkozásoknál kevésbé volt meggyőző: az 508 alany két különböző dózisban kapott az oltóanyagból, és az egyik csoport 59 százaléka, míg a másiknak csak 47 százaléka termelt semlegesítő antitesteket.
Az önkéntesek túlnyomó része 18 és 44 év közötti volt, de így is akadt 13 százaléknyi 55 év fölötti alany, az ő esetükben azonban mindkét dóziscsoportban alacsony volt az antitesttermelés, ami nem túl biztató annak fényében, hogy a COVID-19 betegség leginkább az idősebb korosztályt veszélyezteti. A cég mindenesetre hamarosan a harmadik fázist is megkezdheti, amire Oroszországban, Brazíliában, Chilében és Szaúd-Arábiában már 40 ezer önkéntese van – a kínai cégeknek azért kell külföldön tesztalanyok után nézni, mert az országban a szigorú intézkedéseknek köszönhetően túl jól sikerült a járvány megfékezése.
A Sinovac jóval eredményesebb volt a második fázisban: a cég 600 főn végezte el a klinikai vizsgálatok második szakaszát, és a 18 és 59 év közötti alanyoknak a 90 százalékánál megfigyelték a semlegesítő antitestek termelését. A cég Brazíliában kezdheti majd meg a harmadik fázist, ahol az Instituto Butantan nevű kutatóintézettel közösen kezdte el toborozni azt a közel 9000 önkéntest, akik a feltételek szerint koronavírusos betegekkel foglalkozó intézményekben szolgáló egészségügyi dolgozók közül kerülnek ki.
Ahogy a Sinovac, úgy az állami Sinopharm is inaktivált vírust tartalmazó vakcinákkal kísérletezik – ez az a típus, ami például az influenza elleni védőoltások klasszikus megoldása is. A Sinopharm július közepén kezdte meg a 15 ezer önkéntessel induló harmadik klinikai fázist Abu-Dzabiban, ahol az emirátus egészségügyi minisztere kapta meg a legelső dózist az oltóanyagból. Az állami cég elnöke néhány nappal később azt nyilatkozta, hogy ha minden jól megy, az év végére már piacra is dobhatják a vakcinát.
A járványnak nem lesz vége a vakcina megjelenésének pillanatában
A felerősödött jelentőségű részsikerek és a hamar elkészülő vakcina ígérete azonban könnyen hamis reményeket is kelthet, mert azt azért tudni kell, hogy a védőoltás nem fogja azonnal megszüntetni a járványt, és nem lesz egy csapásra minden olyan, amilyen 2020 előtt volt.
A COVID-vakcinák megjelenésének biológiai, logisztikai, erőforrásbeli és technológiai korlátait összefoglaló Atlantic-cikk szerint a jó hír az, hogy míg egyes vírusok (például a HIV) esetében még a szakértők sem nagyon bíznak az univerzális ellenszer kifejlesztésében, addig a SARS-CoV-2 megfelelő oltóanyagának megtalálása csak idő kérdése. A rossz hír pedig az, hogy valószínűleg még jóval több van hátra a világjárványból, mint amennyi eltelt belőle. „Úgy gondolom, hogy a vakcina megjelenésétől kezdve még jó néhány hónapig lesznek komoly fertőzések, de legalább fertőzésveszély” – mondta a lapnak Jesse Goodman, az amerikai gyógyszerfelügyeleti hivatal (FDA) korábbi vezető kutatója.
A védőoltásokat általában egyenesen az izomba adják, amelynek hatására az immunválaszt követően antitestek termelődnek a vérben, a COVID-19-hez hasonló légúti fertőzések viszont az orr és a garat nyálkahártyáján keresztül történnek, és a nyálkahártyákban sokkal nehezebben termelődnek antitestek. Vagyis azt nagyon nehéz lehet elérni, hogy a vírus bekerüljön a szervezetbe, így a vakcina leginkább a mélyebb szövetek, például a tüdő védelmére szolgálhat. A COVID-vakcina tehát nem biztos, hogy véd a koronavírus-fertőzéstől, viszont a súlyos tüdőbetegségek elkerülhetővé válnak általa – véli Kanta Subbarao, a WHO melbourne-i influenzaközpontjának igazgatója.

Az is tény, hogy a legígéretesebbnek tartott, RNS-alapú vakcinajelöltek olyan technológiára épülnek, amelyet korábban még sosem vetettek be engedélyezett oltásnál, így kérdéses, hogy egyáltalán lehetséges-e a kívánt százmilliós vagy akár milliárdos tételben gyártani őket. A 2009-es H1N1-járvány esetében például az okozott problémát, hogy nem volt elég üzem, ahol a hirtelen gyártásba került, óriási mennyiségű oltóanyagot hatékonyan fiolákba tudták volna tölteni. Az adagolási problémák elkerülésére az amerikai szervek több olyan gyárat létesítettek, ahol a kereskedelmi forgalomra kész oltások előállításának több fázisát egyszerre el lehet végezni, az Operation Warp Speed pedig a fiolák és fecskendők gyártóit is támogatja.
Egy teljes ország (főként ha egy Egyesült Államok méretűről van szó) lakosságának beoltása ráadásul igazi logisztikai rémálom. Az USA erre 2009-ben felhúzott egy egészen jól működő, hierarchikus rendszert, csak közbeszólt a valóság: mivel a H1N1-járvány nem sokkal a vakcina megjelenése után hirtelen lecsengésnek indult, a kereslet is jóval csökkent, így csak a lakosság negyedét tudták sikeresen beoltani. Ezt a bevált, a kormánytól az iskolaorvosokig húzódó ellátási láncot ráadásul nem is tartották fenn, mivel egy évtizeden át nem volt rá szükség.
És akkor még nem volt szó arról a dezinformációs káoszról, ami már eddig is jellemezte a járványt, és várhatóan a vakcinák megjelenését is övezi majd. Az illetékes szerveknek ugyanis minden bizonnyal prioritási sorrendet kell majd felállítaniuk, hogy ki kapjon először az oltóanyagból, és ez a sorrend várhatóan nem fog mindenkinek tetszeni – és innentől szabad az út az összeesküvés-elméletek előtt is. A vakcinákat fejlesztő gyógyszeripari cégek tőzsdei manipulációjáról pedig komolyabban vehető szervezetektől is lehet hallani, hát még a konteók rajongóitól.
Az oltásellenesség az egész vakcinaprogram sikerét alááshatja: egy május végi felmérés szerint az amerikaiaknak csak a 49 százaléka biztos abban, hogy beoltatná magát, ha elérhetővé válik egy COVID-vakcina – 20 százalékuk ezt élből elutasítja, további 31 százalék pedig még nem döntötte el. Az FDA iránymutatása szerint a lakosság legalább 50 százalékát be kéne oltani, hogy esély legyen a nyájimmunitás elérésére.
Azt pedig inkább ne is akarjuk elképzelni, hogy ekkora várakozás után mi lesz, ha a sietve engedélyezett vakcina a szélesebb népesség körében nem éri el a várt hatást, és a járvány tovább tombol. Egy ilyen helyzet nemcsak a vakcinákba, de általánosan a közegészségügyi szakértelembe vetett bizalmat is megrengethetné.
Kapcsolódó cikkek a Qubiten:

Az amerikai kormány máris leszerződött százmillió COVID-19 elleni vakcinára a Pfizerrel
Az amerikai kormány eddig is valóságos pénzesőt zúdított a gyógyszercégekre a COVID-19 elleni oltás reményében, de ilyen nagy üzlet még nem köttetett. A Pfizernek és a BioNTechnek 100 millió vakcinát kell leszállítania.

Áttörést hozhat az oxfordi vakcina
Az Oxfordi Egyetem Jenner Intézetében fejlesztett oltóanyag mind antitestes, mind T-sejtes immunválaszt képes kiváltani, a vizsgálati alanyok 70 százalékánál jelentkező enyhébb mellékhatások pedig hétköznapi gyógyszerekkel orvosolhatók.
Ebben a pillanatban több mint 100 különböző védőoltást fejlesztenek világszerte a koronavírus ellen
Bemutatjuk a legígéretesebb oltóanyagokat, elmagyarázzuk az egyes vakcinatípusok hatásmechanizmusát, és elmondjuk, miért kell óvatosan bánni a vakcinák elkészülésének időpontjára vonatkozó becslésekkel.