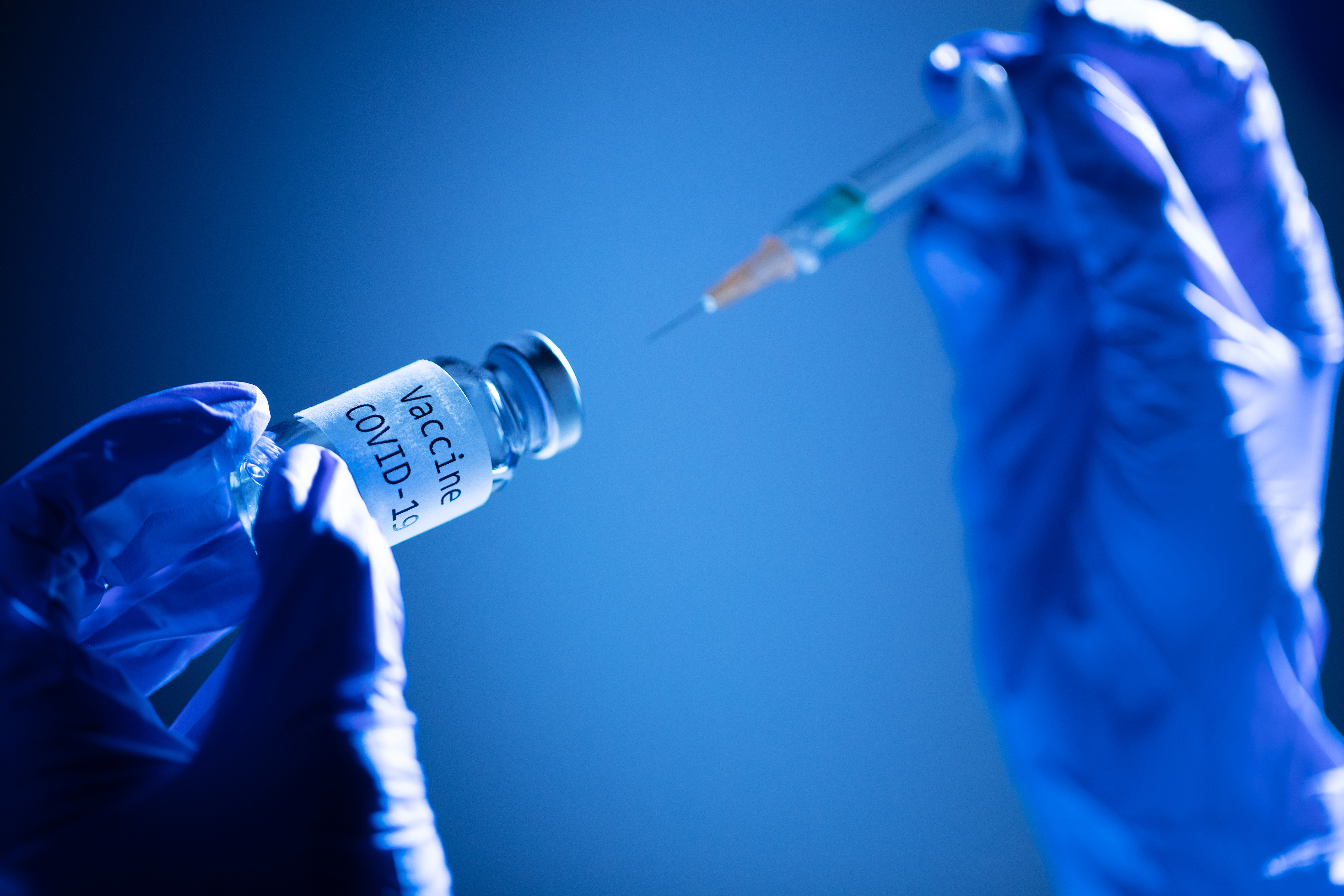
Hogy sikerült csodát művelni és kevesebb mint egy év alatt kifejleszteni a vakcinát a koronavírus ellen?
Az Európai Gyógyszerügynökség (EMA) január hatodikán engedélyezte a Moderna koronavírus elleni vakcináját az Európai Unió területén, míg a Pfizer/BioNTech készítményével már december elején elkezdtek oltani az Egyesült Királyságban, néhány nappal később pedig az Egyesült Államokban is. Az év végén az Oxfordi Egyetem és a brit-svéd AstraZeneca által fejlesztett védőoltásnak is zöld utat adtak a brit hatóságok.
A tudomány óriási teljesítménye, hogy kevesebb mint egy év alatt sikerült kifejleszteni több, különböző oltóanyagot egy korábban ismeretlen vírus ellen, habár ez a teljesítmény akkor válik valóban értékelhetővé, ha az emberek legalább 60 százaléka hajlandó lesz önkéntesen beadatni a vakcinát. Az oltási hajlandóság azonban egyelőre Magyarországon (sok más országgal egyetemben) messze van ettől: az IDEA intézet friss közvélemény-kutatása alapján a megkérdezettek csupán 36 százaléka adatná be magának az oltást, 16 százalékuk egyelőre bizonytalan, a megmaradó 48 százalék pedig egyenesen elutasítja.
Az egyik gyakran hangoztatott, vakcinával szembeni félelem, hogy túl gyorsan fejlesztették ki az oltóanyagot, így kétséges a biztonságossága és a hatásossága. Mivel az IEEE (Institute of Electrical and Electronics Engineers) körképe szerint a vakcinafejlesztés rekordját eddig a mumpsz elleni védőoltás tartotta, amelynek a begyűjtött vírusmintától a piacra dobott termékig mindössze négy évig tartott a kifejlesztése, és átlagosan egy védőoltás biztonságos kikísérletezése 10-15 évet is felölelhet, jogosan merül fel a kérdés, hogyan sikerülhetett ez jelen esetben kevesebb mint egy év alatt.
Segítettek a koronavírusok
Habár az új típusú koronavírust 2019. december 8-án azonosították először a kínai Vuhanban, vizsgálatakor nem a nulláról indultak a kutatók. A SARS-CoV-2 a koronavírusok családjába tartozik, amelynek az amerikai Allergiás és Fertőző Betegségek Nemzeti Intézete szerint több száz tagja van, beleértve azt a négyet is, amelyek a közönséges megfázást okozzák, és azokat is, amelyek a 2002-es SARS-járványt, valamint a 2012-es MERS-járványt szabadították a világra. Eric J. Yager, az Albany Gyógyszer- és Egészségtudományi Egyetem mikrobiológiával foglalkozó adjunktusa a Medical News Today-nek elmondta, a tudósok már több mint 50 éve tanulmányozzák a koronavírusokat, vagyis már a SARS-CoV-2 felbukkanásakor kiterjedt adatbázissal rendelkeztek az ilyen típusú kórokozók genomjairól, struktúráiról és életciklusáról.
A koronavírusok tanulmányozása során derült fény a vírus tüskefehérjéjének jelentőségére az emberi sejtekhez való kapcsolódáskor, és így a tüskefehérjéket már korábban azonosítani tudták, mint az antitestes terápiák és vakcinák potenciális célpontjait – mondta Yager, aki hozzátette, hogy a COVID-19 elleni, adenovírus-alapú Oxford/AstraZeneca-féle oltóanyag alapjait az Oxfordi Egyetem tudósainak a MERS ellen egy adenovírus-alapú vakcina kifejlesztésére tett korai próbálkozásai fektették le.
Világméretű együttműködés és zsákszámra ömlő milliárdok
Normál körülmények között egy vakcina kifejlesztése azért is húzódhat el 10-15 évig, mert a gyógyszerfejlesztés óriási pénzeket ölel fel, és sokszor nincs, aki fedezze a költségeket. Egy 2018-ban a The Lancet Global Health folyóiratban megjelent tanulmány úgy becsülte, hogy az egyes vakcinák kezdeti fejlesztése és a biztonságosság kiderítését célzó korai klinikai vizsgálatok költségei 31-68 millió dollárra tehetők, és a kiterjedt második és harmadik fázisú klinikai vizsgálatok további milliókkal fejelik meg ezeket az összegeket. Az új koronavírus fokozott menetrendjét elnézve ezek a költségek még jobban elszállhattak, így a vakcinák kifejlesztésében döntő jelentőségűek a kormányzati támogatások, a nemzetközi szervezetek és civil alapítványok adományai, valamint a magánszektor befektetései.
Az Európai Bizottság és partnerei 2020. májusában egy nemzetközi adományozói konferencián 9,8 milliárd eurós támogatást kalapoztak össze a vakcinafejlesztésre, ebből csak az Európai Unió 1,4 milliárd eurót adott a koronavírus legyőzésére. Az Egyesült Királyságban a kormányzati Vaccine Taskforce támogatása is hozzátett az Oxford/AstraZeneca vakcinájának kifejlesztéséhez, míg az Operation Warp Speed keretében az Egyesült Államok 456 millió dollárral támogatta a Johnson&Johnson vakcinajelöltjét, több mint 900 millió dollárral a Moderna, mintegy 1,95 milliárd dollárral a Pfizer, valamint körülbelül 1,2 milliárd dollárral az Oxford/AstraZeneca vakcinája kifejlesztését, valamint a védőoltások széles körű gyártását és elosztását.
Emellett a világjárvány nem csupán a pénzcsapokat nyitotta meg, hanem a kutatók közötti együttműködést is serkentette. A géntechnológiában végbement óriási fejlődésnek köszönhetően kínai kutatók már január 11-12-én megosztották a SARS-CoV-2 genomszekvenciáját a nyílt hozzáférésű virological.org oldalon, így a világ tudósai azonnal hozzáláthattak a kórokozó természetének feltérképezéséhez. Emellett számos laboratórium, kutató és gyógyszergyártó cég szinte azonnal átállt a koronavírus elleni vakcina fejlesztésére, a WHO pedig igyekezett a saját eszközeivel sürgetni a globális együttműködést.
Mesterséges intelligencia a kutatólaborban
Számos, a védőoltás talapzatát jelentő vívmányt köszönhetünk a rohamosan fejlődő technológiának, ezek például a már említett géntechnológia, az mRNS-alapú oltások kifejlesztése, valamint a mesterséges intelligenciára törekvő, okos algoritmusok. Ez utóbbiak hónapokkal képesek lerövidíteni a vakcinafejlesztés első, preklinikai szakaszát, ugyanis a kórokozó természetének és viselkedésének pontos megértésén keresztül napokon, sőt órákon belül képesek előállni tesztelhető vakcinajelöltekkel. A világjárvány elején a Bázeli Egyetem kutatói például a Swiss-Model nevű fehérjemodellező eszközt használták arra, hogy megjósolják a SARS-CoV-2 vírus külső burkán lévő fehérjék szerkezetét. A Google tulajdonában álló londoni DeepMind saját, AlphaFold nevű neurális hálóját szintén arra használta, hogy a vírus génszekvenciáját alapul véve kitalálja, hogyan fest a SARS-CoV-2 fehérjék háromdimenziós alakja.
A vakcinagyártók közül számos használt okos algoritmusokat vakcinajelöltje előállításához. Ilyen például a San Diegói Inovio Pharmaceuticals, ahol a cég által bevetett algoritmus három órán belül kidobott egy teljesen megtervezett, optimalizált, DNS-alapú vakcinajelöltet, amely 83 napon belül a klinikai tesztelés fázisába került. Ezen kívül az MIT kutatói gépi tanulással fejlődő algoritmusokat használva terveztek olyan vakcinajelölteket, amelyek különféle populációkra optimalizálhatóak.
Az mRNS-technológia megoldotta a fehérjegyártási problémát
A Karikó Katalin magyar kutató közreműködésével kifejlesztett, hírvivő RNS-en alapuló technológiát a vakcinák történetében először alkalmazzák egy oltóanyag előállításának módszereként. Ez nagyon röviden azt takarja, hogy nanolipid-részecskékbe csomagolva a koronavírus tüskefehérjéjének genetikai örökítőanyagát juttatják be a sejtekbe, és az emberi sejtek ezt az üzenetet használják fel arra, hogy megalkossák saját tüskefehérjéiket. Ezután az immunrendszert a tüskefehérjék segítségével kiképezik a SARS-CoV-2 vírus tüskefehérjéinek jövőbeli felismerésére, a hírvivő RNS pedig, akár egy Snapchat-üzenet, néhány órán vagy napon belül eltűnik a szervezetből.
Shane Crotty, a La Jolla Immunológiai Intézet és a Fertőző Betegségek és Vakcinakutatási Intézet kutatója videóban magyarázta el, hogy az mRNS-technológia a gyártási sebességet tekintve minden más vakcinaelőállítási módszert maga mögé utasít. Crotty szerint a védőoltások előállításának egyik klasszikus módszere, amikor az oltóanyag maga a fehérje, legyen az tüskefehérje vagy virális nanorészecske. Ilyen például a tetanusz vagy a diftéria elleni védőoltás, és néhány koronavírus elleni vakcina esetén is dolgoznak effélén.
Crotty szerint ugyanakkor a fehérjealapú oltások hátulütője, hogy magát a fehérjét kell előállítani, és mindegyik fehérjéhez meg kell találni annak saját előállítási módszerét. Mivel ez minden egyes protein esetén egyedülálló, az engedélyeztetési szerveknek, például az amerikai Élelmiszer- és Gyógyszerfelügyelet (FDA) szakértőinek a gyártási folyamat minden egyes lépését külön felül kell vizsgálniuk, ami jelentősen megnyújthatja az engedélyeztetési procedúrát. Ráadásul a vírusok fehérjéi általában szokatlan proteinek, így nem könnyű legyártani őket; a folyamat rengeteg időt és energiát vesz igénybe.
A professzor szerint ezzel szemben a hírvivő RNS-alapú vakcináknál nem áll fenn ez a probléma, mivel a gyártási folyamat minden esetben ugyanaz. Bár az RNS maga különböző szekvenciákat kódol, molekuláris szempontból a gyártási folyamata ugyanaz, így a vakcina engedélyeztetése nagyon gyorsan megtörténhet, mivel a gyógyszerfelügyeleti hatóságoknak csak egyfajta gyártási módszert kell felülvizsgálniuk. Tudományos szempontból Crotty szerint ez közrejátszott abban, hogy az egyes vakcinajelöltek ennyire gyorsan végigmentek az első, második és harmadik klinikai tesztelési fázison.
Kapcsolódó cikkek a Qubiten:
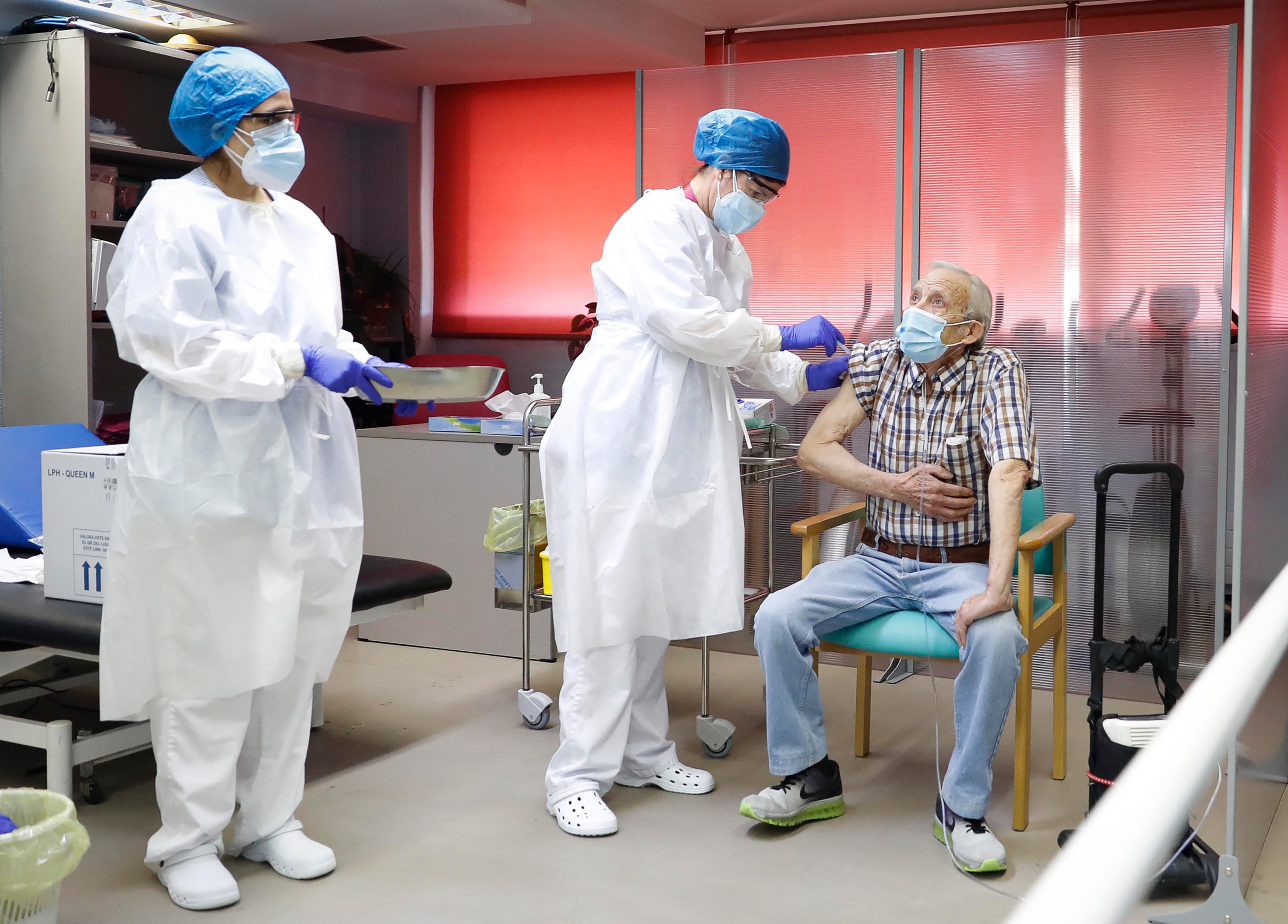
MTA-kutatóorvosok: Mindenki oltassa be magát koronavírus ellen, aki teheti!
A SARS-CoV-2 elleni védőoltással szembeni fenntartások nem támaszthatók alá semmilyen orvostudományi megfigyeléssel. A legtöbbször megalapozatlan és tudománytalan hírek rontják a védőoltásba vetett bizalmat, és súlyosan veszélyeztetik a járvány leküzdésének lehetőségét – írta az MTA ötven orvosa.

Annak is érdemes beadatni az oltást, aki már átesett a COVID-19-en
Aki az egyik fajta oltóanyagból kapta az első adagot, kaphatja-e a másodikat egy másik vakcinából? Aki részt vett a vakcinakísérletekben, kapjon-e a piacra kerülő oltásból? A Manchesteri Egyetem immunológusa három alapvető kérdést tárgyalt a piacra kerülő vakcinákkal kapcsolatban.

A mesterséges intelligencia gőzerővel keresi a vakcinát a koronavírus ellen
Az okos algoritmusok hónapokkal képesek csökkenteni a vakcinafejlesztéshez szükséges időt, és ez kulcsfontosságú a járvány elleni versenyfutásban. Persze az AI sem mindenható, a koronavírus-vakcina embereken történő tesztelését például egyáltalán nem válthatja ki.
Kapcsolódó cikkek