Hamisított eredményekre alapozhatták az elmúlt 16 év Alzheimer-kutatásainak jó részét

Az Alzheimer-kór az időskori demencia leggyakoribb fajtája, amely először a kognitív funkciók romlásával, majd gyors biológiai leépüléssel jár. A demencia, amely eseteinek 60-80 százalékáért az Alzheimer-kór felel, a hetedik helyen áll a világ vezető halálokai között. Világszerte legalább 50 millióan szenvednek a leginkább 65 év felett jelentkező kórtól, míg Magyarországon becslések szerint minimum 250 ezer embert érinthet a betegség, de a szakértők szerint az esetek háromnegyedében ezt nem diagnosztizálják.
Bár a betegséget már több mint száz éve, 1906-ban leírta Alois Alzheimer német pszichiáter és kollégája, a megelőzésére és kezelésére irányuló kutatások a 21. században pörögtek fel igazán, és az elmúlt évtizedben a korábbinál jelentősen bőkezűbb finanszírozásban részesül a terület. Ez többek között olyan nagy hatású tanulmányoknak köszönhető, mint a Nature-ben 2006 márciusában megjelent, a Minnesotai Orvosi Egyetem kutatóinak vezetésével közölt írás, amely egérkísérletekre alapozva vezette fel a későbbi Alzheimer-kutatások irányát erősen befolyásoló elméletet, miszerint az Aβ*56 nevű molekula lehet a kognitív leépülés kulcsa, ezért a gyógyszerkutatások során is annak mechanizmusára érdemes koncentrálni.
Csakhogy a Science magazin idén júliusban egy fél éven át tartó vizsgálat után arra jutott, hogy a 16 éves tanulmány központi elemeit manipulálhatták, hogy azok jobban alátámasszák a kutatók hipotézisét. A hamisított adatok és a manipulált felvételek ráadásul nemcsak erre az egy tanulmányra jellemzők, hanem az egyik szerző, a Minnesotai Egyetem idegtudósaként dolgozó Sylvain Lesné legalább 20 másik tanulmányában találtak képmanipulációra utaló nyomokat, több mint 70 felvétel esetében.
A Nature egyelőre a 2006-os kutatás felülvizsgálatára figyelmeztető szöveggel látta el a több mint 2200-szor idézett tanulmányt, de a Minnesotai Egyetem is vizsgálódik az ügyben. Ha beigazolódik a manipuláció, akkor Lesné gyakorlatilag egy személyben felelne több milliárd dollár elégetéséért, rengeteg potenciálisan hamis diagnózisért és másfél évtizednyi idő elvesztegetéséért az elöregedő világban egyre több embert érintő betegség gyógymódjának kutatásában.
A manipulált adatok úgy mennek át a legnagyobb kutatókon is, mint kés a vajon
A botrány kirobbanásához is egy klinikai vizsgálattal kapcsolatban felmerült aggályok vezettek el. Matthew Schrag, a nashville-i Vanderbilt Egyetem idegtudósa egy bírósági ügyben vett részt szakértőként, és a manipulált képek azonosításával igazolta a felperesek állítását, miszerint a Cassava Sciences nevű gyógyszeripari cég Simufilam nevű kísérleti Alzheimer-gyógyszerével folytatott vizsgálatok hamisított kutatási eredményeken alapulnak. Schrag szerint a Simufilammal végzett (egyébként a mai napig folyamatban lévő) klinikai vizsgálatok résztvevőit úgy teszik ki a mellékhatások kockázatainak, hogy közben nincs valódi esély a gyógyulásra.
Schrag és a Science magazin további vizsgálatai nyomán száznál is több manipulált képet találtak mérvadó Alzheimer-kutatásokban, és az ezek közül több mint 70-et elkövető Sylvain Lesné munkássága került a botrány középpontjába. A tudományos publikációk fotómanipulálásainak észlelésére szakosodott molekuláris biológus, Elisabeth Bik szerint „úgy tűnt, hogy az ábrákat különböző kísérletekből származó fényképek részleteinek összerakásával állították össze”. A szakértő szerint elképzelhető, hogy a kapott kísérleti eredmények nem feleltek meg a hipotézisnek, ezért utólag ahhoz igazították az adatokat és a képeket.
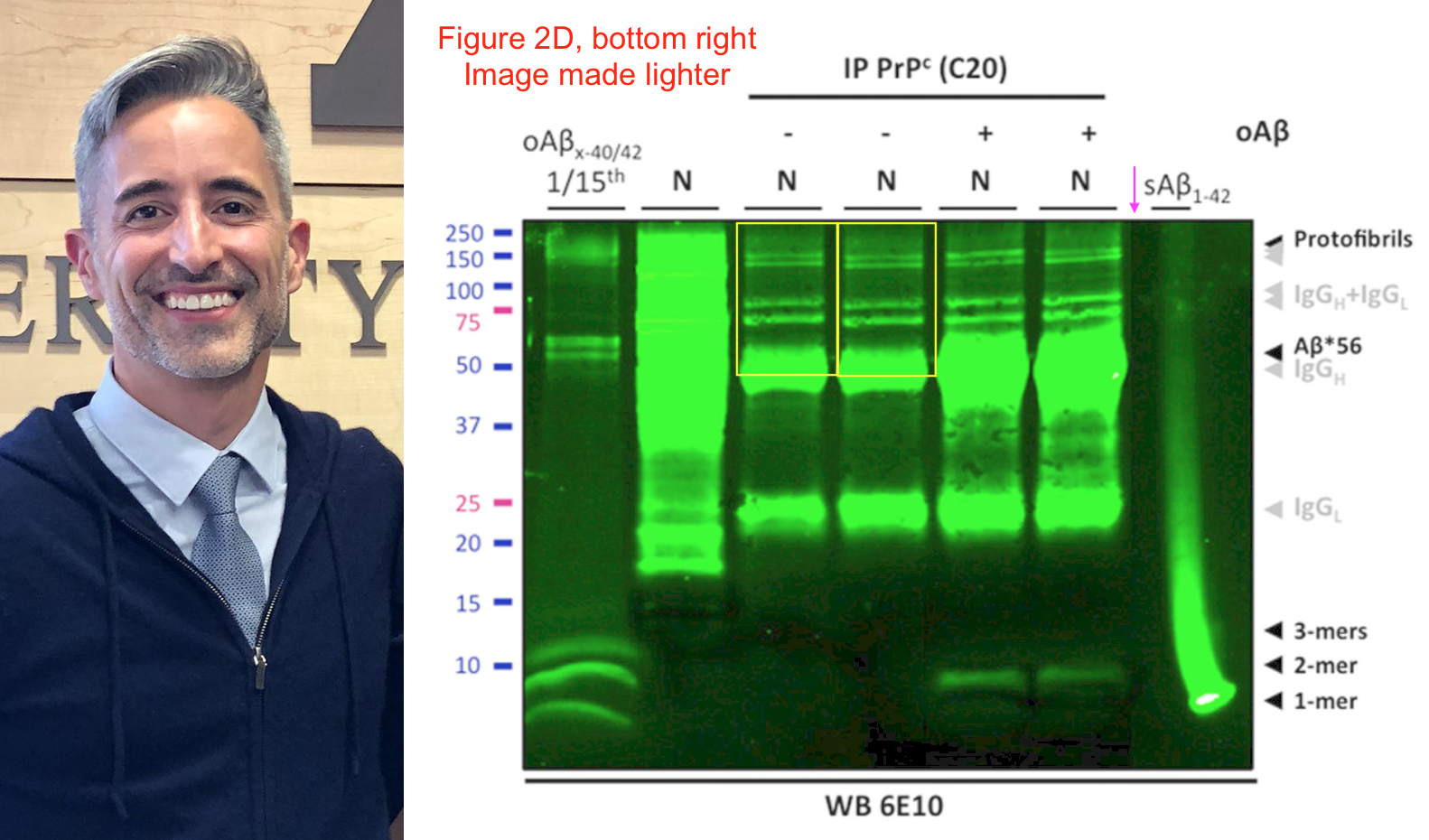
Több kutató már régóta gyanakszik Lesné munkásságára, ugyanis az Aβ*56 molekula nem igazán akart feltűnni más alzheimeres mintákban. Dennis Selkoe, a Harvard Alzheimer-kutatója a Science-nek elmondta, hogy 2008-ban kétszer is megpróbálkozott a molekula azonosításával emberi szövetekben és testnedvekben, de nem járt sikerrel. Most, hogy szembesítették a manipulációval, Selkoe elismeri, hogy hibás kutatási irányt követett – pedig ő maga is 13 alkalommal hivatkozott publikációiban a 2006-os Nature-tanulmányra.
A tudományos publikációk szakmai elbírálásának (peer review) folyamatára és a szkepticizmus természetére jól rámutat, hogy a Science-cikk megjelenése után az AlzForum felületén tucatjával jelentek meg a világ Alzheimer-kutatói, hogy elmondják, már régóta kételkedtek Lesné kutatásaiban, az Aβ*56 létezésében vagy egyáltalán a béta-amiloidok fontosságában. És ezzel minden bizonnyal nem voltak egyedül (a PubPeeren már 2013-ban felfedeztek Lesné-féle képmanipulálást), de az, hogy ennek idáig nem adtak hangot, felveti a kérdést, hogy mennyire lehet hinni a szakmai konszenzusban.
„Az ilyen hamisítások egészen biztosan egyre nagyobb teret nyernek, hiszen óriási a publikációs kényszer, a nagy nevű újságok egyre nagyobb mennyiségű kísérleti adatot követelnek, a gyógyszerfejlesztések esetén pedig erre még nagyon komolyan rátevődik a konkrét anyagi érdek is. Ez persze az alapkutatásnál is megvan, hiszen a nagy cikkekkel lehet csak jelentős pályázatokat elnyerni. Sajnos ez alapjaiban kérdőjelezi meg a tudomány hitelességét, a közölt adatok megalapozottságát. Még rosszabb, hogy az ábrák manipulálása önmagában még nem jelenti azt, hogy csak az ezeken alapuló állítások lehetnek hamisak. Sokszor ugyanis a nem manipulált ábra is lehet hazugság, például ha a 10-szer megismételt kísérlet közül pont azt az egy eredményt mutatják be, amit a másik 9 cáfolt, azaz hamis következtetést vonnak le” – mondta a Qubitnek Schlett Katalin neurobiológus, az ELTE TTK Élettani és Neurobiológiai Tanszékének vezetője.
Az Alzheimer-kutatásba ömlik a pénz, miközben egyre több a botrány
Bár kutatási manipulációkkal tele a padlás – ahogy azt a PubPeer vagy a Retraction Watch létezése is bizonyítja –, ez a konkrét hamisítási botrány azért is kavart nagy port a tudományos közösségben, mert az Alzheimer-kutatás az elmúlt évtizedben az egyik legnagyobb pénzügyi támogatást élvező területté nőtte ki magát. Míg 2008-ban az amerikai orvostudományi kutatásokat finanszírozó Nemzeti Egészségügyi Intézetek (NIH) teljes büdzséjének 1,4 százaléka (530 millió dollár) jutott Alzheimer-kutatásokra, 2019-ben már a 6,1 százaléka (2,4 milliárd dollár), így az összes részterület közül a legnagyobb, 352 százalékos emelkedést produkálta.
„Az Alzheimer-kórral kapcsolatos kutatásokra, mind az alap-, mind pedig a gyógyszerfejlesztésre koncentráló kutatások terén óriási pénzeket fordítanak, részben a hatalmas társadalmi igény, illetve a jelenleg még hiányzó hatásos gyógymód miatt” – mondta Schlett Katalin. Éppen ez a magas finanszírozás lehet az oka annak, hogy az évtizedek óta viszonylag sikertelen Alzheimer-kutatás területét átszövik a botrányok.
„Pont tavaly volt nagy botrány abból, hogy az FDA az ellentmondásos és hiányos klinikai eredmények ellenére, gyanús körülmények mellett és gyorsított módon engedélyezett egy monoklonális ellenanyag-terápiát [Aduhelm], ami évtizedek óta az első terápiás kezelést jelentené az alzheimeres betegeknek. Ez az eljárás is az amiloid plakkokat célozná, ugyanakkor az alapkutatásban, részben az ellentmondásos kísérleti adatok miatt is, elég régóta elterjedt a kritikája annak az elképzelésnek, hogy a betegséget a plakk-képzés befolyásolásán keresztül hatékonyan lehetne gyógyítani” – mondta Schlett.
Milyen hatással lesz ez az eset az Alzheimer-kutatásra és a tudományos közösségre?
Az Alzheimer-kutatások gyógyszerfejlesztési irányvonalát már évtizedek óta az úgynevezett amiloid hipotézis határozza meg. Eszerint a kór kialakulását elsősorban a béta-amiloid fehérjék felhalmozódása okozza: a hipotézis szerint ezek a fehérjék a strukturális különbségeik miatt könnyebben tapadnak össze, így csomószerűen, plakkok formájában rakódnak le az agyban, ahol előidézik az idegsejtek pusztulását.
Ez az elképzelés azonban már korántsem áll olyan biztos lábakon, mint egy-két évtizede. Klinikai vizsgálatok során ugyanis kiderült, hogy a béta-amiloid fehérjék szintje nem áll összefüggésben a betegség súlyosságával, vagy hogy az amiloid plakkok a demencia tünetét egyáltalán nem mutató emberek agyában is megtalálhatók (és fordítva: demens emberek agyában néha egyáltalán nincs nyomuk), és amíg anti-béta-amiloid immunterápiával már sikerült eltávolítani ilyen plakkokat egerekkel és emberekkel végzett kísérletekben is, kognitív javulást egyszer sem sikerült ezzel a módszerrel elérni.
Mindezek ellenére kutatók sokasága óva int attól, hogy teljesen elvessük az amiloid hipotézist, annak sikerét ugyanis szerintük nem lehet kizárólag a klinikai vizsgálatok alapján megítélni. A University College London demenciakutató intézetének gyógyszerfelfedezéssel is foglalkozó kutatója, Paul Whiting szerint a technikai problémák mellett a legnagyobb gondot az okozhatja az ilyen klinikai teszteknél, hogy a kezelést a betegség túl késői szakaszában kezdik meg, ugyanis a népszerű elmélet szerint az Alzheimer-kór kialakulása a tünetek megjelenése előtt évekkel elkezdődhet.
A Stanford Egyetem molekuláris és sejtfiziológusa, Thomas Südhof az Intelligencer kérdésére elmondta, az továbbra sem lehet kérdés, hogy „a béta-amiliod plakkok fontos markerei az Alzheimer-kórnak, inkább abban nincs egyetértés, hogy azok önmagukban vezetnek a betegséghez, vagy csak a kórt kiváltó események nagyobb együttesének részei”. A 2013-ban orvosi Nobel-díjjal kitüntetett kutató szerint ezért a manipuláció feltárásának nem lesz nagy hatása az Alzheimer-kutatások irányára, legfeljebb a klinikai teszteknél mellőzik a kérdéses Aβ*56 molekulát.
Schlett Katalin is hasonlóképp látja a helyzetet: „Önmagában ez a jelenlegi cikkmanipulálási botrány az alapkutatásban szerintem nem rengethette meg jelentősen a folyó kutatásokat. Kicsit cinikusan szólva, aki eddig hitt benne, az továbbra is kitarthat az elképzelése mellett, bár a nagy sajtóvisszhang egészen biztosan kihat a tudományos lapok szerkesztőire, és valószínűleg a jövőben nehezebb lesz olyan közleményeket elfogadtatni, amik támogatják ezt az elképzelést.”
Karl Herrup, a Pittsburghi Egyetem agykutató intézetének neurobiológusa az NBC-nek fejtette ki, hogy szerencsére nem csak Lesné munkáira alapultak az elmúlt másfél évtized Alzheimer-kutatásai (többek között az agyszöveti gyulladásra koncentráló irány lehet ígéretes), de az ilyen esetek mindig óriási károkat okoznak a tudományos közösségnek, és aláássák az emberek tudományba vetett bizalmát. „A tudományban sosem szégyen tévedni. A legnagyobb tudományos eredmények jó része úgy született, hogy az emberek tévedtek, bebizonyították, hogy valóban tévedtek, majd azt is, hogy miért tévedtek. Ami teljesen mérgező a tudományra nézve, az a csalás” – mondta Herrup.
Kapcsolódó cikkek a Qubiten:
Miért bukik el újra és újra az Alzheimer-kór elleni harc?
2050-re 100 millióan lesznek a világon, akik Alzheimer-kór okozta demenciában szenvednek, mégis siralmas a betegséget célzó gyógyszerkísérletek statisztikája,. A kudarcban közrejátszhat, hogy a kór szakemberek szerint már évtizedekkel azelőtt elkezdődhet, hogy megjelennének az első tünetek. Azért léteznek biztató új kutatási irányok.

Meglepően sok kutató trükközik vagy csal a tudományos eredményekkel
Hatvanezer kutatót hívtak meg minden idők legnagyobb tudományos integritásról szóló felmérésére, de sok egyetem vonakodott részt venni benne, így végül csak 6800 kutató vallott az általa alkalmazott praktikákról. Kiderült, hogy a publikációs kényszer szüli a trükkös megoldásokat, és mivel az egész rendszert nem lehet újraírni, csak bizonyos jó gyakorlatok bevezetése segíthet.

Válságban van a modern tudomány, de létezik kiút belőle
Hibás kutatási eredmények, replikációs krízis, SHARKing, közlési kényszer, ragadozó kiadványok ezrei: milyen problémákkal küzd napjainkban a tudományos élet, és hogyan lehet megoldani őket?